题目内容
某化学兴趣小组在实验室做了有关金属的实验,并将实验过程及涉及到的所有物质用如下流程图表示.
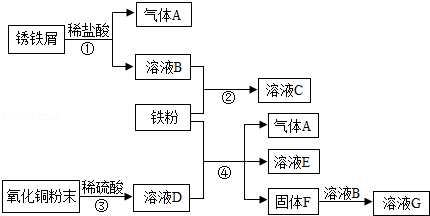
(1)铁屑生锈的原因是 .
(2)写出过程①中铁锈溶解反应的化学方程式: .
(3)过程②发生化合反应使溶液由黄色变为浅绿色,则该反应的化学方程式是 .
(4)溶液E的溶质一定含有 (填化学式).
(5)除氧化铜粉末外,实验过程所涉及的物质中,一定含有铜元素的有 (填字母序号).
【答案】
(1)铁屑与空气中的氧气、水蒸气等发生化学反应;
(2)Fe2O3+6HCl═2FeCl3+3H2O;(3)2FeCl3+Fe═3FeCl2;(4)FeSO4;(5)DFG.
【解析】
试题分析:(1)铁在有水和氧气并存时易生锈,故填:铁屑与空气中的氧气、水蒸气等发生化学反应;
(2)铁锈溶解是因为铁锈的主要成分氧化铁与盐酸反应生成了氯化铁和水,故填:Fe2O3+6HCl═2FeCl3+3H2O;(3)B中含有盐酸、氯化铁和氯化亚铁,过程②发生化合反应使溶液由黄色变为浅绿色,则是铁与氯化铁反应生成了氯化亚铁,故填:2FeCl3+Fe═3FeCl2;(4)D中含有硫酸铜,硫酸铜能与铁反应生成硫酸亚铁和铜,故溶液E中一定含有硫酸亚铁,故填:FeSO4;(5)氧化铜与硫酸反应得到的B中含有硫酸铜,硫酸铜与铁反应得到的固体F为铜,F与溶液B反应得到的溶液G中含有氯化铜,故填:DFG.
考点:物质的鉴别、推断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
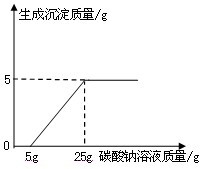 某化学兴趣小组在用石灰石(杂质不与酸反应,也不溶于水)或稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他们决定利用该废液测定这瓶Na2CO3溶液的溶质质量分数.他们先将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示.
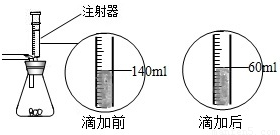
某化学兴趣小组在用石灰石(杂质不与酸反应,也不溶于水)或稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他们决定利用该废液测定这瓶Na2CO3溶液的溶质质量分数.他们先将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示.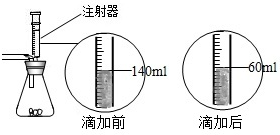 某化学兴趣小组在实验课上制取二氧化碳气体选择了下图的发生装置.在制取完毕后有同学提出该装置还能测得稀盐酸的质量分数.小娜同学称取12.5g含CaCO380%的石灰石粉末样品置于装置中,用注射器滴加稀盐酸至恰好完全反应,滴加前后的数据如如图所示:(杂质与稀盐酸不反应,稀盐酸的密度为1.25g/mL)
某化学兴趣小组在实验课上制取二氧化碳气体选择了下图的发生装置.在制取完毕后有同学提出该装置还能测得稀盐酸的质量分数.小娜同学称取12.5g含CaCO380%的石灰石粉末样品置于装置中,用注射器滴加稀盐酸至恰好完全反应,滴加前后的数据如如图所示:(杂质与稀盐酸不反应,稀盐酸的密度为1.25g/mL)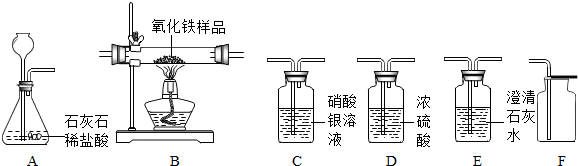
 某化学兴趣小组在实验课上制取二氧化碳气体选择了下图的发生装置.在制取完毕后有同学提出该装置还能测得稀盐酸的质量分数.小娜同学称取12.5g含CaCO380%的石灰石粉末样品置于装置中,用注射器滴加稀盐酸至恰好完全反应,滴加前后的数据如如图所示:(杂质与稀盐酸不反应,稀盐酸的密度为1.25g/mL)
某化学兴趣小组在实验课上制取二氧化碳气体选择了下图的发生装置.在制取完毕后有同学提出该装置还能测得稀盐酸的质量分数.小娜同学称取12.5g含CaCO380%的石灰石粉末样品置于装置中,用注射器滴加稀盐酸至恰好完全反应,滴加前后的数据如如图所示:(杂质与稀盐酸不反应,稀盐酸的密度为1.25g/mL)