题目内容
将铁粉和铜粉的混合物7 g,加入到盛有58.1 g稀盐酸的烧杯中,恰好完全反应。此时烧杯内各物质的总质量为64.9 g。试计算:
(1)原混合物中铁粉的质量分数;
(2)反应后所得溶液中溶质的质量分数;
(3)配制上述反应中所用稀盐酸需要质量分数为38%的浓盐酸(密度为1.19 g/cm3)的体积。(计算结果精确到0.1)
【解析】生成H2的质量为7 g+58.1 g-64.9 g=0.2 g
设原混合物中Fe的质量为x,生成FeCl2的质量为y,参加反应的HCl的质量为z。
Fe+2HCl====FeCl2+H2↑
56 73 127 2
x z y 0.2 g
56∶2=x∶0.2 g x=5.6 g
127∶2=y∶0.2 g y=12.7 g
73∶2=z∶0.2 g z=7.3 g
(1)原混合物中铁粉的质量分数为: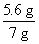 ×100%=80%
×100%=80%
(2)反应后所得溶液中溶质的质量分数为: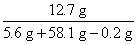 ×100%=20%
×100%=20%
(3)需要38%的浓盐酸的体积为:7.3 g÷38%÷1.19 g/cm3≈16.1 mL

练习册系列答案
相关题目
 请回答下列有关金属的问题:
请回答下列有关金属的问题: