题目内容
过氧化钠(Na202)是淡黄色粉末,在通常状况下能跟许多物质发生化学反应。例如:2Na2O2+2H20==4NaOH+02↑ 2Na202+2C02==2Na2C03+02
2Na202+4HCl==4NaCl+2H20+02↑
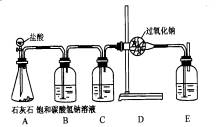
为了验证C02跟Na2O2反应产生的气体是O2,某同学设计了如图所示的实验装置。
试回答下列问题:
(1)设计B、C装置的目的是净化C02气体。其中,B装置的作用是 :C装置的作用是 ,瓶内液体是 ;如果将B、C两瓶内所盛的液体互换,直接的后果是 。
(2)E装置的作用是 ,瓶内液体应是 ,所发生反应的化学方程式是 。
(3)为了验证CO2跟Na202反应产生的气体是O2,最后还要进行的实验操作是 。
答案:
提示:
提示:
| (1)根据题给信息,为了达到“验证C02跟Na2O2反应产生的气体是O2”的实验目的,必须除去C02气体中的HCL气体和H20(g),所以B装置的作用是除去C02中的HCl气体,C装置的作用是除去CO2 中的水蒸气,瓶内液体装浓H2S04,如果将B、C两瓶内所盛的液体互换,直接的后果是通向D装置中的C02气体中仍有水蒸气。
(2)E装置的作用是吸收未反应的C02,目的是便于检验出02,吸收C02可NaOH溶液,反应方程式为 (3)检验02可用带火星的小木条靠近E装置中的导气管,若复燃则为O2
|

练习册系列答案
相关题目
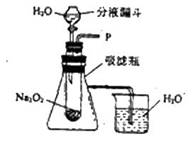
 【实验装置】如右图所示
【实验装置】如右图所示