题目内容
6.实验室中某些同学将28g铁粉加入100g稀盐酸中恰好完全反应,求:(1)产生氢气的质量;
(2)稀盐酸中溶质的质量分数.
分析 铁与稀盐酸反应生成氯化亚铁,同时放出氢气,根据铁粉的质量即可求出氢气的质量和氯化氢的质量,进而求稀盐酸中溶质的质量分数.
解答 解:设产生氢气的质量为x,盐酸中氯化氢的质量为y
Fe+2HCl═FeCl2 +H2↑
56 73 2
28g y x
$\frac{56}{28g}=\frac{73}{y}=\frac{2}{x}$
x=1g,y=36.5g
(1)产生氢气的质量为1g;
(2)稀盐酸中溶质的质量分数:$\frac{36.5g}{100g}×100%$=36.5%
答:稀盐酸中溶质的质量分数为36.5%.
点评 此题是根据化学方程式进行计算的考查题,注意过程要规范,计算要准确.

练习册系列答案
相关题目
16.化学物质正逐渐改变我们的生活,下列有关说法不正确的是( )
| A. | 为保障食品安全,应杜绝使用食品添加剂 | |
| B. | 为防止骨质疏松,人体每日应摄入足够量的钙 | |
| C. | 用二氧化碳灭火器扑灭图书、档案等物的失火 | |
| D. | 为了可持续发展,不仅要善用金属材料和制品,更要有计划地开采金属资源 |
17.各种洗涤剂广泛进入人们的生活中,下列所用的洗涤剂不具有乳化作用的是( )
| A. | 用沐浴露洗澡 | B. | 用洗衣粉洗衣服 | ||
| C. | 用洗洁精洗餐具上的油污 | D. | 用汽油洗去手上的油污 |
14.某市的空气质量日报如下表:
请根据表中的数据分析,填写下列空白.
(1)造成该城市空气污染的物质主要是有害气体和烟尘.
(2)空气污染指数与空气质量之间的关系是:空气污染指数越小,空气质量越好.
(3)表中没有列出二氧化碳的量,是因为二氧化碳不属于空气污染气体,不被列入监测范围.
(4)由表中数据可知,冬季时空气中各种污染物含量明显高于其他季节,你认为原因可能是:冬季取暖,大量燃烧煤炭.
(5)请你提出一条降低冬季空气污染物含量的合理建议:减少煤的使用.
| 2015年5月1日 | 2015年12月1日 |
| 二氧化硫 33 一级 一氧化碳 39 一级 二氧化氮 35 一级 可吸入颗粒物 32 一级 | 二氧化硫 63 二级 一氧化碳 59 二级 二氧化氮 61 二级 可吸入颗粒物 68 二级 |
(1)造成该城市空气污染的物质主要是有害气体和烟尘.
(2)空气污染指数与空气质量之间的关系是:空气污染指数越小,空气质量越好.
(3)表中没有列出二氧化碳的量,是因为二氧化碳不属于空气污染气体,不被列入监测范围.
(4)由表中数据可知,冬季时空气中各种污染物含量明显高于其他季节,你认为原因可能是:冬季取暖,大量燃烧煤炭.
(5)请你提出一条降低冬季空气污染物含量的合理建议:减少煤的使用.
1.下列实验事实不能用质量守恒定律解释的是( )
| A. | 蜡烛在空气中燃烧后质量减轻 | |
| B. | 铁块放置在空气中一段时间后质量增加了 | |
| C. | 冰融化成水前后质量没变 | |
| D. | 煤燃烧后的剩余物的质量比煤的质量小 |
5.完成下表(按氧化物、酸、碱、盐分类填写)
| 物质名称(或俗称) | 熟石灰 | 纯碱 | 硫酸 | ||
| 化学式 | CuSO4•5H2O | CaO | |||
| 分类 |
2.化学概念在逻辑上有如图所示关系时,对下列概念间的关系说法正确的是( )
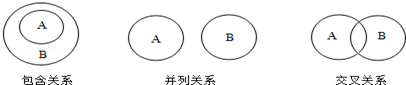
①纯净物与混合物属于包含关系
②化合物与氧化物属于包含关系
③单质与化合物属于交叉关系
④酸、碱、盐属于并列关系
⑤中和反应与复分解反应属于并列关系.

①纯净物与混合物属于包含关系
②化合物与氧化物属于包含关系
③单质与化合物属于交叉关系
④酸、碱、盐属于并列关系
⑤中和反应与复分解反应属于并列关系.
| A. | ①② | B. | ③④ | C. | ①⑤ | D. | ②④ |
3.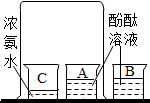 在课堂上,老师和同学们共同完成了如图所示实验,容器A中溶液变红,B中溶液不变色,该实验现象说明( )
在课堂上,老师和同学们共同完成了如图所示实验,容器A中溶液变红,B中溶液不变色,该实验现象说明( )
 在课堂上,老师和同学们共同完成了如图所示实验,容器A中溶液变红,B中溶液不变色,该实验现象说明( )
在课堂上,老师和同学们共同完成了如图所示实验,容器A中溶液变红,B中溶液不变色,该实验现象说明( )| A. | 分子可以分成原子,原子不能再分 | |
| B. | 分子在不断地运动,温度越高运动越快 | |
| C. | 氨气溶于水后溶液呈碱性 | |
| D. | 分子是化学变化中的最小微粒 |