��Ŀ����
ˮ����������������������أ�ijʵ��С�鷢��ʵ�����еõ�������ˮ�ʻ�ɫ������ζ����ˮ�����ǣ��й���С�������ֶ�ˮ���������´�����
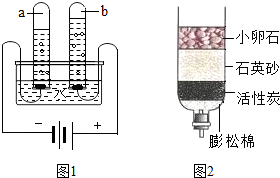
����ˮ���м��������������ܽ⣬���ó�������________����������ƣ����ɵõ���Һ��
����������Һ�м������̿��������________���ó�ȥˮ���е���ɫ����ζ���ù�������________�仯�����������ѧ������
��������ˮ���Ƿ������ԣ���ѡ��________��________��
��С��ͬѧ����һ�����͵�����ˮ������X����ˮ������������ҵ����ȡX �Ļ�ѧ����ʽΪ��Cl2+2NaClO2�T2NaCl+2X����X�Ļ�ѧʽΪ________��NaClO2����Ԫ�صĻ��ϼ�Ϊ________��
������������Ӧ������2molCl2 ���뷴Ӧ����ɲ���NaCl________�ˣ���д����ʽ����Ĺ��̣�
���� ���� ���� ʯ����Һ pH��ֽ ClO2 +3 234
�������������е�֪ʶ���з���������ʱ���벻���Թ����Һ��ķ���������̿���������ԣ�������ɫ�غ���ζ��Ҫ������Һ������ԣ�����ʹ�����ָʾ����pH��ֽ�����������غ㶨�ɣ���ѧ��Ӧǰ��Ԫ�ص������ԭ�ӵĸ������䣬�����Ƶ�X�Ļ�ѧʽ�����ݻ��ϼ۹��������û�������ijԪ�صĻ��ϼۣ����ݷ�Ӧ�Ļ�ѧ����ʽ��������μӷ�Ӧ���Ȼ��Ƶ����ʵ������������������
��𣺢�Ҫ��ȥˮ�еIJ����Թ��壬����ʹ�ù��˵ķ�����������ˣ�
�ڻ���̿���������ԣ�������ɫ�غ���ζ���˹�����û�������µ����ʣ����������仯�����������������
�ۼ���ˮ���Ƿ�����ԣ����Ը���������ʽ��У�������Һ��ʹʯ����Һ��죬������Һ��pHС��7�����ʯ����Һ��pH��ֽ��
�����ݷ�Ӧ�Ļ�ѧ����ʽ��Cl2+2NaClO2�T2NaCl+2X����Ӧǰ����4��Clԭ�ӣ�2��Naԭ�ӣ�4��Oԭ�ӣ���Ӧ������2��Naԭ�ӣ�2��Clԭ�ӣ���2X�к���2��Clԭ�Ӻ�4��Oԭ�ӣ���X�к���1��Clԭ�Ӻ�2��Oԭ�ӣ��仯ѧʽΪClO2��
����Ԫ�صĻ��ϼ�Ϊx�����У�+1��+x+��-2����2=0�����x=+3��
���ClO2��+3��
���������Ȼ��Ƶ����ʵ���Ϊx
Cl2+2NaClO2�T2NaCl+2ClO2
1 2
2mol x

x=4mol
�Ȼ��Ƶ�����Ϊ4mol��58.5g/mol=234g
���234��
���������⿼���˾�ˮ��֪ʶ�Լ������غ㶨�ɵ�Ӧ�ã���ɴ��⣬�����������е�֪ʶ���У�
�������������е�֪ʶ���з���������ʱ���벻���Թ����Һ��ķ���������̿���������ԣ�������ɫ�غ���ζ��Ҫ������Һ������ԣ�����ʹ�����ָʾ����pH��ֽ�����������غ㶨�ɣ���ѧ��Ӧǰ��Ԫ�ص������ԭ�ӵĸ������䣬�����Ƶ�X�Ļ�ѧʽ�����ݻ��ϼ۹��������û�������ijԪ�صĻ��ϼۣ����ݷ�Ӧ�Ļ�ѧ����ʽ��������μӷ�Ӧ���Ȼ��Ƶ����ʵ������������������
��𣺢�Ҫ��ȥˮ�еIJ����Թ��壬����ʹ�ù��˵ķ�����������ˣ�
�ڻ���̿���������ԣ�������ɫ�غ���ζ���˹�����û�������µ����ʣ����������仯�����������������
�ۼ���ˮ���Ƿ�����ԣ����Ը���������ʽ��У�������Һ��ʹʯ����Һ��죬������Һ��pHС��7�����ʯ����Һ��pH��ֽ��
�����ݷ�Ӧ�Ļ�ѧ����ʽ��Cl2+2NaClO2�T2NaCl+2X����Ӧǰ����4��Clԭ�ӣ�2��Naԭ�ӣ�4��Oԭ�ӣ���Ӧ������2��Naԭ�ӣ�2��Clԭ�ӣ���2X�к���2��Clԭ�Ӻ�4��Oԭ�ӣ���X�к���1��Clԭ�Ӻ�2��Oԭ�ӣ��仯ѧʽΪClO2��
����Ԫ�صĻ��ϼ�Ϊx�����У�+1��+x+��-2����2=0�����x=+3��
���ClO2��+3��
���������Ȼ��Ƶ����ʵ���Ϊx
Cl2+2NaClO2�T2NaCl+2ClO2
1 2
2mol x

x=4mol
�Ȼ��Ƶ�����Ϊ4mol��58.5g/mol=234g
���234��
���������⿼���˾�ˮ��֪ʶ�Լ������غ㶨�ɵ�Ӧ�ã���ɴ��⣬�����������е�֪ʶ���У�

��ϰ��ϵ�д�
�����Ŀ
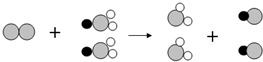
 ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ� ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ� ��ʾ��ԭ�ӣ�
��ʾ��ԭ�ӣ�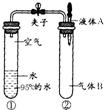
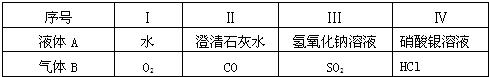
 2012��3��22���ǵڶ�ʮ�조����ˮ�ա���ˮ����������������������أ�
2012��3��22���ǵڶ�ʮ�조����ˮ�ա���ˮ����������������������أ� ˮ����������������������أ���ش��������⣮
ˮ����������������������أ���ش��������⣮