题目内容
侯氏制碱法的主要反应为:NH3+CO2+H2O+NaCl=NaHCO3+NH4Cl.一定温度下,向92.6g饱和NaCl溶液中先通入足量NH3,再通入一定量CO2发生反应,若参加反应的NH3质量为3.4g,请计算:(写出计算步骤,不考虑溶解在溶液中的NH3和CO2的质量).
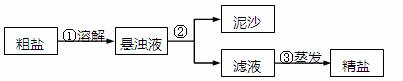
(1)消耗CO2的质量是多少
(2)反应后称量溶液中析出NaHCO3晶体的质量为11.8g,则剩余溶液的质量是多少?
(3)求剩余溶液中NaHCO3的质量分数(计算结果精确到0.1%)。
练习册系列答案
相关题目
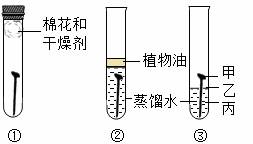
下列实验方案不能达到相应目的的是
| A | B | C | D | |
| 实验方案 |
|
|
|
|
| 目的 | 证明呼出气体比吸入空气的CO2含量多 | 证明氨分子在不断运动 | 检查装置的气密性 | 测定空气中氧气的含量 |