题目内容
18.通过一年来对化学的学习,我们应该树立的理念是( )| A. | 化学是自然科学中创造新物质最多的科学领域 | |
| B. | 化学的发展是环境恶化的罪魁祸首 | |
| C. | 化学是以理论推导为基础的科学 | |
| D. | 推广食用不含任何化学物质的“绿色食品” |
分析 A、根据化学的定义和用途判断.
B、根据化学的作用判断.
C、根据化学的特点分析.
D、绿色食品是指绿色植物通过光合作用转化的食品.
解答 解:A、利用化学可以开发新能源和新材料,以改善人类生存的条件,所以正确.
B、化学为人类提供了丰富的生活和生产资料,化学在科学中发挥着越来越重要的作用;合理利用化学,可防止环境恶化,故说法错误.
C、化学是以实验研究为基础的科学,所以错误.
D、绿色食品中一定含有化学物质;所以错误.
故选A.
点评 化学是研究物质的组成、结构、性质及其变化规律的科学,我们研究物质的目的是为了应用,了解化学的用途有利于培养学习兴趣,提高社会责任感.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
8.20℃时,NaCl溶解于水的实验数据如下表.则下列叙述正确的是( )
| 实验序号 | ① | ② | ③ | ④ |
| 水的质量(g) | 10 | 10 | 10 | 10 |
| 加入NaCl的质量(g) | 2 | 3 | 4 | 5 |
| 溶液的质量(g) | 12 | 13 | 13.6 | 13.6 |
| A. | ②中所得溶液是饱和溶液 | B. | 20℃时10g水最多能溶解4gNaCl | ||
| C. | ③④溶液的浓度相同 | D. | ④溶液是不饱和溶液 |
6.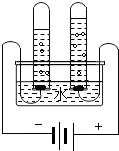 如图为验证水的组成的实验装置,下列有关说法正确的是( )
如图为验证水的组成的实验装置,下列有关说法正确的是( )
 如图为验证水的组成的实验装置,下列有关说法正确的是( )
如图为验证水的组成的实验装置,下列有关说法正确的是( )| A. | 正极和负极产生的气体质量比为1:2 | |
| B. | 正极产生的气体能使带火星的木条复燃 | |
| C. | 水是由一个氧元素和两个氢元素组成的 | |
| D. | 该变化中的最小粒子为氢分子和氧分子 |
3.如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆圈代表不同的原子.下列说法正确的是( )
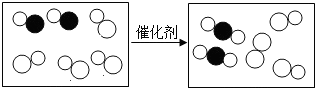

| A. | 此反应有单质生成 | |
| B. | 原子在化学变化中是可分的 | |
| C. | 此反应有三种新物质生成 | |
| D. | 参加反应的两种分子的个数比为2:1 |
7.下列有关碳和碳的氧化物的说法错误的是( )
| A. | 金刚石和石墨的物理性质不同,是因为它们的碳原子排列方式不同 | |
| B. | 一氧化碳和二氧化碳的组成元素相同,所以它们的化学性质相似 | |
| C. | 木炭和活性炭都具有吸附性 | |
| D. | 二氧化碳用于灭火,即利用它的物理性质也利用了它的化学性质 |
8.今年春季,我省部分地区雨水较少,出现了旱情,为了增强农作物的抗旱能力,小明建议父母施用适量的磷肥,下列化肥中属于磷肥的是( )
| A. | K2SO4 | B. | CO(NH2)2 | C. | Ca3(PO4)2 | D. | KNO3 |