题目内容
发射“神舟七号”载人航天飞船的火箭用偏二甲肼和四氧化二氮(N2O4)作常规推进剂,其完全反应的化学反应方程式为:偏二甲肼+2N2O4=3N2+2CO2+4H2O,则下列叙述错误的是( )
| A、偏二甲肼的化学式是C2H8N2 |
| B、偏二甲肼中碳元素与氢元素的质量比为1:4 |
| C、偏二甲肼的一个分子中共有12个原子 |
| D、偏二甲肼中氮元素的质量分数约为46.7% |
考点:化学式的书写及意义,元素质量比的计算,元素的质量分数计算
专题:化学用语和质量守恒定律
分析:A、根据质量守恒定律来分析解答;B、根据计算化合物中元素质量比的方法来分析解答;C、根据物质的化学式来分析解答;D、根据化合物中元素的质量分数来分析解答.
解答:解:A、由反应偏二甲肼+2N2O4=3N2+2CO2+4H2O,根据质量守恒定律可知,反应前后元素的种类、原子的种类和个数不变,O原子个数在反应前后相等,反应后共2个C原子、6个N原子、8和H原子,则反应前应共有2个C原子、6个N原子、8和H原子,反应前已有4个N原子,则一个偏二甲肼分子中中应有2个C原子、2个N原子、8个H原子,则偏二甲肼的化学式为C2H8N2;
B、根据偏二甲肼的化学式C2H8N2可知,碳元素与氢元素的质量比为:(12×2):(1×8)=3:1;
C、根据偏二甲肼的化学式C2H8N2可知,1个偏二甲肼分子中含有2个碳元素、8个氢原子和2个氮原子,共12个原子;
D、偏二甲肼中,氮元素的质量分数为:
×100%≈46.7%.
故选B.
B、根据偏二甲肼的化学式C2H8N2可知,碳元素与氢元素的质量比为:(12×2):(1×8)=3:1;
C、根据偏二甲肼的化学式C2H8N2可知,1个偏二甲肼分子中含有2个碳元素、8个氢原子和2个氮原子,共12个原子;
D、偏二甲肼中,氮元素的质量分数为:
| 14×2 |
| 12×2+1×8+14×2 |
故选B.
点评:考查了质量守恒定律的应用、化学式的意义及其相关计算,难度较小.

练习册系列答案
相关题目
下列物质的名称、俗名与化学式完全正确对应的是( )
| A、氢氧化钠 火碱 NaOH |
| B、碳酸氢钠、纯碱、NaHCO3 |
| C、氢氧化钙 熟石灰 CaO |
| D、氯化钠、食盐、NaCl2 |
氧化亚铜(Cu2O)是一种鲜红色粉末状固体.在氧化亚铜中铜元素的化合价为( )
| A、-1 | B、-2 | C、+1 | D、+2 |
下列变化属于化学变化的是( )
| A、纸张燃烧 | B、冰雪融化 |
| C、水分蒸发 | D、矿石粉碎 |
学习化学时会遇到一些与“相等”有关的规律,下列有关“相等”的说法中错误的是( )
| A、在原子中原子核内的质子数一定等于核外电子数 |
| B、中和反应中参加反应的酸和碱的质量一定相等 |
| C、溶液稀释前后,溶质的质量一定相等 |
| D、物质发生化学变化前后,元素的种类数一定相等 |
 如图,“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下丁可以转化为乙.下面四组选项中,符合如图要求的是如图,“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下丁可以转化为乙.下面四组选项中,符合如图要求的是( )
如图,“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下丁可以转化为乙.下面四组选项中,符合如图要求的是如图,“-”表示相连的物质间在一定条件下可以反应,“→”表示在一定条件下丁可以转化为乙.下面四组选项中,符合如图要求的是( )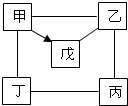 如图中“--”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以转化为戊,甲、乙、丙、丁、戊分别为Mg、MgO、H2SO4、NaOH、CuCl2五种物质中的一种,回答下列问题:
如图中“--”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以转化为戊,甲、乙、丙、丁、戊分别为Mg、MgO、H2SO4、NaOH、CuCl2五种物质中的一种,回答下列问题: