题目内容
请根据下列实验装置图回答问题: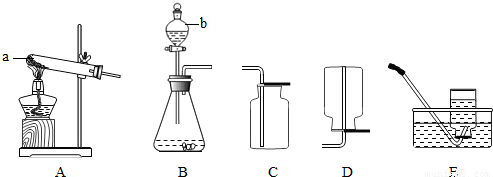
(1)写出标号仪器名称:a ,b .
(2)实验室用B、E装置制取氧气的化学方程式是 ,反应的基本类型为 反应.若反应较为剧烈,为了减缓反应,可采取的措施是 .若要检验氧气,则需 .
(3)实验室制取二氧化碳的化学方程式是 ,选用的收集装置为 (填装置序号)
(4)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气的发生装置为 (填装置序号)
收集应选用D装置,把收集满氨气的集气瓶倒扣在水中,观察到集气瓶内有大量水进入.根据上述信息则下列推测合理的有 (填序号).
①氨气的密度比空气小;②氨气的密度比空气大;③氨气易溶于水;④氨气不溶于水.
【答案】分析:(1)根据常用仪器即可判断;
(2)实验室用B装置制取氧气,不需加热,据此判断所用药品,书写反应方程式,并依据反应特点判断反应类型;并依据仪器用途、氧气的性质分析解答后面的问题;
(3)根据二氧化碳的实验室制法书写化学方程式,依据二氧化碳的性质确定收集装置;
(4)根据发生装置和收集装置的选择条件即可判断.
解答:解:(1)标号仪器分别是试管和分液漏斗;
故答案为:试管;分液漏斗;
(2)实验室用B装置制取氧气,属于固体和液体不加热制气体,可以发现用双氧水及二氧化锰制取氧气符合条件,方程式是:2H2O2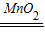 2H2O+O2↑,该反应由一种物质分解生成两种物质,属于分解反应;分液漏斗可逐滴滴加液体,所以若反应较为剧烈,为了减缓反应,可采取的措施是:控制分液漏斗滴加液体的速度;检验氧气用带火星的木条伸入瓶内,观察是否复燃进行判断;
2H2O+O2↑,该反应由一种物质分解生成两种物质,属于分解反应;分液漏斗可逐滴滴加液体,所以若反应较为剧烈,为了减缓反应,可采取的措施是:控制分液漏斗滴加液体的速度;检验氧气用带火星的木条伸入瓶内,观察是否复燃进行判断;
故答案为:2H2O2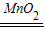 2H2O+O2↑;分解;控制分液漏斗滴加液体的速度;将带火星的木条伸入集气瓶内,若木条复燃则是氧气;
2H2O+O2↑;分解;控制分液漏斗滴加液体的速度;将带火星的木条伸入集气瓶内,若木条复燃则是氧气;
(3)实验室制取二氧化碳是用大理石和稀盐酸反应制取,大理石的主要成分碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳能溶于水,密度大于空气,故只能用向上排空气法收集;
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;C;
(4)加热氯化铵和氢氧化钙固体混合物可制取氨气,发生装置属于固体和固体加热制气体,故选发生装置A;收集应选用D装置,说明氨气的密度比空气小,把收集满氨气的集气瓶倒扣在水中,观察到集气瓶内有大量水进入,说明氨气易溶于水;
故答案为:A;①③.
点评:此题重在考查同学们对常用化学仪器的了解和识记情况,并且要掌握常用气体的发生装置和收集装置的选取方法,以及方程式的书写,实验注意事项,才能正确解题.
(2)实验室用B装置制取氧气,不需加热,据此判断所用药品,书写反应方程式,并依据反应特点判断反应类型;并依据仪器用途、氧气的性质分析解答后面的问题;
(3)根据二氧化碳的实验室制法书写化学方程式,依据二氧化碳的性质确定收集装置;
(4)根据发生装置和收集装置的选择条件即可判断.
解答:解:(1)标号仪器分别是试管和分液漏斗;
故答案为:试管;分液漏斗;
(2)实验室用B装置制取氧气,属于固体和液体不加热制气体,可以发现用双氧水及二氧化锰制取氧气符合条件,方程式是:2H2O2
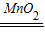 2H2O+O2↑,该反应由一种物质分解生成两种物质,属于分解反应;分液漏斗可逐滴滴加液体,所以若反应较为剧烈,为了减缓反应,可采取的措施是:控制分液漏斗滴加液体的速度;检验氧气用带火星的木条伸入瓶内,观察是否复燃进行判断;
2H2O+O2↑,该反应由一种物质分解生成两种物质,属于分解反应;分液漏斗可逐滴滴加液体,所以若反应较为剧烈,为了减缓反应,可采取的措施是:控制分液漏斗滴加液体的速度;检验氧气用带火星的木条伸入瓶内,观察是否复燃进行判断;故答案为:2H2O2
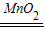 2H2O+O2↑;分解;控制分液漏斗滴加液体的速度;将带火星的木条伸入集气瓶内,若木条复燃则是氧气;
2H2O+O2↑;分解;控制分液漏斗滴加液体的速度;将带火星的木条伸入集气瓶内,若木条复燃则是氧气;(3)实验室制取二氧化碳是用大理石和稀盐酸反应制取,大理石的主要成分碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳能溶于水,密度大于空气,故只能用向上排空气法收集;
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;C;
(4)加热氯化铵和氢氧化钙固体混合物可制取氨气,发生装置属于固体和固体加热制气体,故选发生装置A;收集应选用D装置,说明氨气的密度比空气小,把收集满氨气的集气瓶倒扣在水中,观察到集气瓶内有大量水进入,说明氨气易溶于水;
故答案为:A;①③.
点评:此题重在考查同学们对常用化学仪器的了解和识记情况,并且要掌握常用气体的发生装置和收集装置的选取方法,以及方程式的书写,实验注意事项,才能正确解题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目






