题目内容
某化学兴趣小组利用以下装置探究气体的制取及性质.请结合如图回答有关问题:
(1)写出装置中仪器①的名称 .
(2)可通过加热二氧化锰和氯酸钾混合物制取氧气,反应中二氧化锰的作用是 ;该反应的化学方程式是 .
(3)实验室制取并收集二氧化碳的装置组合是 (填字母);用G装置吸收二氧化碳气体时气体应从 (填“长”或“短”)导管口进入.
(4)实验室可用铜片与稀硝酸反应制取一氧化氮(NO)气体,已知一氧化氮有毒,难溶于水,常温下极易与氧气发生反应(2NO+O2═2NO2),制取一氧化氮的收集装置为 (填字母).
(5)不能用C装置干燥的气体是 (填字母).
a.氧气 b.氢气 c.氨气 d.二氧化碳气体.
【答案】分析:(1)依据常用仪器回答;
(2)二氧化锰是氯酸钾分解的催化剂,反应生成氯化钾和氧气,据此书写方程式;
(3)据实验室制取二氧化碳的反应物的状态和反应条件选择发生装置,据二氧化碳的密度和溶解性选择收集装置,用G装置吸收二氧化碳气体时气体应长进短出;
(4)据一氧化氮的密度和溶解性选择收集装置;
(5)氨气可与硫酸反应,不能用浓硫酸干燥.
解答:解:(1)仪器①是长颈漏斗;
(2)二氧化锰是氯酸钾分解的催化剂,反应生成氯化钾和氧气,方程式是2KClO3 2KCl+3O2↑;
2KCl+3O2↑;
(3)实验室制取二氧化碳用大理石和稀盐酸常温反应,属于固液常温型,故选发生装置A,二氧化碳密度比空气大且能溶于水,用向上排空气法收集;用G装置吸收二氧化碳气体时气体应长进短出;
(4)一氧化氮有毒,难溶于水,常温下极易与氧气发生反应(2NO+O2═2NO2),故只能用排水法收集;
(5)氨气可与硫酸反应,不能用浓硫酸干燥;
故答案为:(1)长颈漏斗;
(2)催化剂;2KClO3 2KCl+3O2↑;
2KCl+3O2↑;
(3)AE;长;
(4)D;
(5)c.
点评:掌握氯酸钾制取氧气的反应方程式,并能据反应物的状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,干燥气体所用干燥剂不能与被干燥的气体发生反应.
(2)二氧化锰是氯酸钾分解的催化剂,反应生成氯化钾和氧气,据此书写方程式;
(3)据实验室制取二氧化碳的反应物的状态和反应条件选择发生装置,据二氧化碳的密度和溶解性选择收集装置,用G装置吸收二氧化碳气体时气体应长进短出;
(4)据一氧化氮的密度和溶解性选择收集装置;
(5)氨气可与硫酸反应,不能用浓硫酸干燥.
解答:解:(1)仪器①是长颈漏斗;
(2)二氧化锰是氯酸钾分解的催化剂,反应生成氯化钾和氧气,方程式是2KClO3
 2KCl+3O2↑;
2KCl+3O2↑;(3)实验室制取二氧化碳用大理石和稀盐酸常温反应,属于固液常温型,故选发生装置A,二氧化碳密度比空气大且能溶于水,用向上排空气法收集;用G装置吸收二氧化碳气体时气体应长进短出;
(4)一氧化氮有毒,难溶于水,常温下极易与氧气发生反应(2NO+O2═2NO2),故只能用排水法收集;
(5)氨气可与硫酸反应,不能用浓硫酸干燥;
故答案为:(1)长颈漏斗;
(2)催化剂;2KClO3
 2KCl+3O2↑;
2KCl+3O2↑;(3)AE;长;
(4)D;
(5)c.
点评:掌握氯酸钾制取氧气的反应方程式,并能据反应物的状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,干燥气体所用干燥剂不能与被干燥的气体发生反应.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
某化学兴趣小组利用下列装置进行O2、CO2的实验室制法和有关性质的研究.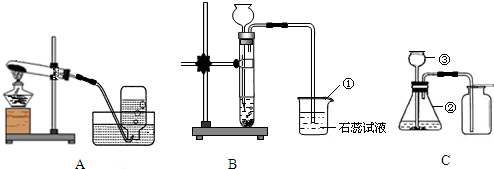
(1)写出下列编号仪器的名称:① ;② ③
(2)甲同学要用KMnO4固体来制取O2,应选用上图中的 装置(填编号).用化学方程式表示反应原理 .当O2收集满,取出集气瓶后,停止该实验的正确操作步骤是先 ,后 .
(3)为了较准确测定KMnO4完全分解产生氧气的体积,可进行以下试验:称取9.5g KMnO4加热直至无气体放出,过一会儿读取进入量筒里的气体体积.试完成下列填空:测量气体体积时,可以将反应发生装置和收集装置中的气体冷却至室温再进行.则收集气体应选下图中的装置 才合理(填编号),理由是 .
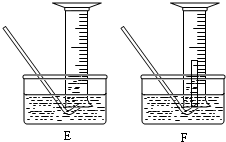
(4)乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红.对这一变化的合理解释是 (填序号)
A、产生的CO2直接使石蕊试液变红
B、产生的CO2与水反应生成H2CO3使石蕊试液变红
C、挥发出的氯化氢溶于水使石蕊试液变红
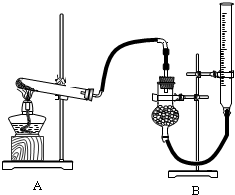
(5)实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解,现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较,用下图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表
:
回答下列问题:
①上述实验中的“待测数据”指 ;
②本实验装置图中量气装置B由球形干燥管、乳胶管和50mL滴定管(带刻度)改造后组装而成,此处所用液体通常选 (填字母编号);
A、水;B、浓硫酸;C、双氧水;D、无水酒精
③若要证明实验②中球形干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞, ,观察现象;
④为探究CuO在实验
(6)中是否起催化作用,需补做如下实验(无需写出具体操作):
A、 B、CuO的化学性质有没有改变.

(1)写出下列编号仪器的名称:①
(2)甲同学要用KMnO4固体来制取O2,应选用上图中的
(3)为了较准确测定KMnO4完全分解产生氧气的体积,可进行以下试验:称取9.5g KMnO4加热直至无气体放出,过一会儿读取进入量筒里的气体体积.试完成下列填空:测量气体体积时,可以将反应发生装置和收集装置中的气体冷却至室温再进行.则收集气体应选下图中的装置

(4)乙同学用浓盐酸和大理石在B装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红.对这一变化的合理解释是
A、产生的CO2直接使石蕊试液变红
B、产生的CO2与水反应生成H2CO3使石蕊试液变红
C、挥发出的氯化氢溶于水使石蕊试液变红
(5)实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解,现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较,用下图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表
:

| 实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
| ④ | 1.2g | 无其它物质 | |
| ⑤ | 1.2g | CuO0.5g | |
| ⑥ | 1.2g | MnO20.5g |
①上述实验中的“待测数据”指
②本实验装置图中量气装置B由球形干燥管、乳胶管和50mL滴定管(带刻度)改造后组装而成,此处所用液体通常选
A、水;B、浓硫酸;C、双氧水;D、无水酒精
③若要证明实验②中球形干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,
④为探究CuO在实验
(6)中是否起催化作用,需补做如下实验(无需写出具体操作):
A、
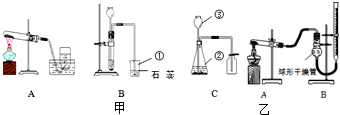
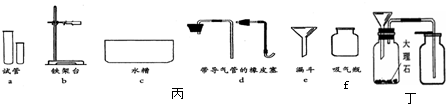
 某化学兴趣小组利用下列仪器进行实验,以探究仪器的对功能性.
某化学兴趣小组利用下列仪器进行实验,以探究仪器的对功能性. 某化学兴趣小组利用下列仪器进行实验,以探究仪器的对功能性.
某化学兴趣小组利用下列仪器进行实验,以探究仪器的对功能性.
