题目内容
 小明同学在某化工厂进行社会实践,技术员与小明一起分析由氯化钙和氯化钠组成的产品中氯化钠的含量。现取13.4g固体样品,全部溶于96.6g水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如右图所示的曲线关系。技术员提示小明:氯化钙与碳酸钠反应的化学方程式
小明同学在某化工厂进行社会实践,技术员与小明一起分析由氯化钙和氯化钠组成的产品中氯化钠的含量。现取13.4g固体样品,全部溶于96.6g水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如右图所示的曲线关系。技术员提示小明:氯化钙与碳酸钠反应的化学方程式 是
是 CaCl2+Na2CO3=CaCO3↓+2NaCl。求:
CaCl2+Na2CO3=CaCO3↓+2NaCl。求:
⑴当氯化钙与碳酸钠恰好完全反应时,消耗10.6%的碳 酸钠溶液的质量是 g。
⑵当氯化钙与碳酸钠恰好完全反应时,过滤,所得溶液中溶质的质量分数是多少?
解:(1)100g
(2)由生成沉淀的质量曲线, 当氯化钙与碳酸钠恰好完全反应时,消耗10.6%的碳酸钠溶液的质量为100g;设样品中碳酸钠的质量为x,生成氯化钠的质量为y
当氯化钙与碳酸钠恰好完全反应时,消耗10.6%的碳酸钠溶液的质量为100g;设样品中碳酸钠的质量为x,生成氯化钠的质量为y
CaCl2+Na2CO3═CaCO3↓+2NaCl
106 100
x 10g
106 100

 ==
==
X 10 g
解得:x=10.6g
原样品中的氯化钠质量为:13.4g-10.6g=2.8 g
所得溶液中溶质的质量分数是(2.8g+11.7g/13.4 g +96.6 g +100g )×100%=6.9%
答:所得溶液中溶质的质量分数是6.9%.

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
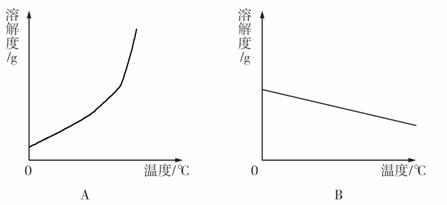
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是 (填A或B)。
(2)要想把一 瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰。
其中措施正确的是 。
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g 饱和NaO H溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为 。
H溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为 。
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数 乙 甲(填“>”、“<”或“=”)。
(5)现有60℃时含Ca(OH)2和N aOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是 。
aOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是 。
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH (填“偏大”、“偏小”或“不受影响”)。
“凤凰”号火星探测器圆满完成任务,向地面发回数量堪称史无前例的图像和数据,为人类探索火星提供了宝贵的科学资料。请完成14~16题。
(1) “凤凰”号探测器发回的最新照片上显示,火星上确有液态水存在。下列微粒模型示意图可表示构成水的微粒的是 (填标号)。
a. b.
b. c.
c. d.
d.
(2)火星上含有丰富的二氧化碳和镁资源。科学家设想,镁可作为未来火星上的燃料,因为镁能在二氧化碳中燃烧放出大量的热,同时生成氧化镁和碳。该反应的化学方程式为 。
(3)火星北极的土壤呈弱碱性。如果火星具备作物生长的条件,下表所列作物较适宜在火星北极种植的有 。
| 作物名称 | 芦笋 | 草莓 | 萝卜 | 马铃薯 |
| 适宜生长的pH | 5.5~7.8 | 5.5~6.5 | 5~8 | 5.6~6 |
