题目内容
请回答下列问题:
(1)用CO高温下还原赤铁矿(主要成份Fe2O3)的化学方程式为:
(2)金属镁着火不能用CO2灭火,因为镁能在CO2中燃烧生成碳和氧化镁.该反应的化学方程式为
(3)食物中的糖类给人体提供热量,某糖X在人体内发生的反应是:X+6O2═6CO2+6H2O,则X的化学式为
(4)如图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图.
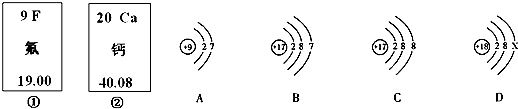
①钙元素的原子序数为
②A、B、C、D中属于同种元素的粒子是
③A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似
(1)用CO高温下还原赤铁矿(主要成份Fe2O3)的化学方程式为:
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
| ||
(2)金属镁着火不能用CO2灭火,因为镁能在CO2中燃烧生成碳和氧化镁.该反应的化学方程式为
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
,反应基本类型是
| ||
置换反应
置换反应
.(3)食物中的糖类给人体提供热量,某糖X在人体内发生的反应是:X+6O2═6CO2+6H2O,则X的化学式为
C6H12O6
C6H12O6
;判断的依据是质量守恒定律
质量守恒定律
.(4)如图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图.

①钙元素的原子序数为
20
20
;图D中X=8
8
;②A、B、C、D中属于同种元素的粒子是
BC
BC
(填序号);③A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似
B
B
(填序号).分析:(1)CO高温下还原赤铁矿(主要成份Fe2O3)生成铁和二氧化碳,写出反应的化学方程式即可.
(2)镁能在CO2中燃烧生成碳和氧化镁,写出该反应的化学方程式即可.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
(4)①根据元素周期表中的一格中获取的信息,元素符号前面的数字表示原子序数;根据原子中核电荷数=核内质子数,进行分析解答.
②根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数),据此进行分析解答.
③根据元素的化学性质跟它的原子的最外层电子数目有关,决定元素的化学性质的是原子的最外层电子数,进行分析解答.
(2)镁能在CO2中燃烧生成碳和氧化镁,写出该反应的化学方程式即可.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
(4)①根据元素周期表中的一格中获取的信息,元素符号前面的数字表示原子序数;根据原子中核电荷数=核内质子数,进行分析解答.
②根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数),据此进行分析解答.
③根据元素的化学性质跟它的原子的最外层电子数目有关,决定元素的化学性质的是原子的最外层电子数,进行分析解答.
解答:解:(1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO
2Fe+3CO2.
(2)镁能在CO2中燃烧生成碳和氧化镁,该反应的化学方程式为:2Mg+CO2
2MgO+C;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
(3)根据反应的化学方程式X+6O2═6CO2+6H2O,反应物中氧原子个数分别为12,反应后的生成物中碳、氢、氧原子个数分别为6、12、18,根据反应前后原子种类、数目不变,则每个X分子由6个碳原子、12个氢原子和6个氧原子构成,则物质X的化学式为C6H12O6.
(4)①根据元素周期表中的一格中获取的信息,钙元素的原子序数为20;原子中核电荷数=核内质子数,18=2+8+X,X=8.
②根据决定元素种类的是核电荷数(即核内质子数),因为B、C的核内质子数相同,所以B、C属于同种元素的粒子.
③决定元素的化学性质的是原子的最外层电子数,A粒子B粒子的最外层电子数相同,A粒子化学性质与B粒子化学性质相似.
故答案为:(1)Fe2O3+3CO
2Fe+3CO2;(2)2Mg+CO2
2MgO+C;置换反应;(3)C6H12O6;质量守恒定律;(4)①Cl-;②BC;③B.
| ||
(2)镁能在CO2中燃烧生成碳和氧化镁,该反应的化学方程式为:2Mg+CO2
| ||
(3)根据反应的化学方程式X+6O2═6CO2+6H2O,反应物中氧原子个数分别为12,反应后的生成物中碳、氢、氧原子个数分别为6、12、18,根据反应前后原子种类、数目不变,则每个X分子由6个碳原子、12个氢原子和6个氧原子构成,则物质X的化学式为C6H12O6.
(4)①根据元素周期表中的一格中获取的信息,钙元素的原子序数为20;原子中核电荷数=核内质子数,18=2+8+X,X=8.
②根据决定元素种类的是核电荷数(即核内质子数),因为B、C的核内质子数相同,所以B、C属于同种元素的粒子.
③决定元素的化学性质的是原子的最外层电子数,A粒子B粒子的最外层电子数相同,A粒子化学性质与B粒子化学性质相似.
故答案为:(1)Fe2O3+3CO
| ||
| ||
点评:本题难度不大,掌握化学方程式的书写方法、利用原子守恒来确定物质的化学式的方法、元素周期表中元素的信息是正确解答本题的关键.

练习册系列答案
相关题目
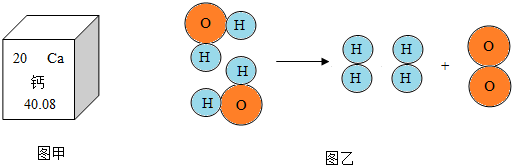

 该微粒的符号为
该微粒的符号为