题目内容
将氧化铜和三氧化二铁混合均匀的混合物a g分成两等分,向其中一份混合物中加入b%的硫酸溶液c g恰好完全溶解,将另一份混合物在过量的一氧化碳气流中加热充分反应,求冷却后剩余固体的质量.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:金属氧化物与硫酸反应生成硫酸盐和水,根据硫酸的物质的量可知金属氧化物中O元素的物质的量,金属氧化物的质量减去氧的质量即为金属的质量.
解答:解:由反应CuO~H2SO4~H2O,Fe2O3~3H2SO4~3H2O,根据质量守恒定律,反应前后质量不变,可知硫酸中氢元素的质量为b%?cg×
,水中氧元素的质量为氧化铜和三氧化二铁中氧元素的质量,水中氧元素的质量为b%?cg×
÷
×
,若将
g原混合物在足量CO中加热,使其充分反应,冷却后剩余固体为金属单质,则质量为氧化物的质量减去氧的质量,为
g-b%?cg×
÷
×
=
g-
?b%?c.
答案:冷却后剩余固体的质量
g-
?b%?c.
| 2 |
| 98 |
| 2 |
| 98 |
| 2 |
| 18 |
| 16 |
| 18 |
| a |
| 2 |
| a |
| 2 |
| 2 |
| 98 |
| 2 |
| 18 |
| 16 |
| 18 |
| a |
| 2 |
| 8 |
| 49 |
答案:冷却后剩余固体的质量
| a |
| 2 |
| 8 |
| 49 |
点评:本题考查混合物的计算,题目难度不大,本题注意根据反应的特点,确定金属氧化物与硫酸反应的关系式,从而得出硫酸的物质的量与金属氧化物中O元素的物质的量相等,此为解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质属于氧化物的是( )
| A、O2 |
| B、CO |
| C、KClO3 |
| D、NaOH |
在托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别加入50g溶质质量分数为7.3%的稀盐酸,将天平调节至平衡;然后向左右两烧杯中分别加入一定质量的下列各组物质,充分反应后,天平发生偏转的是( )
| A、1.8g铝粉和1.8g 铁粉 |
| B、4.2g碳酸镁和2g硝酸银 |
| C、5.6g铁粉和5.6g 锌粉 |
| D、10g碳酸钙和5.6g氧化钙 |
氧气跟世间万物如影随形.下列关于氧气说法正确的是( )
| A、用带火星的木条可以检验氧气 |
| B、碳在氧气中燃烧产生淡蓝色火焰,并有使澄清石灰水变浑浊的气体产生 |
| C、氧气可用于动植物呼吸、医疗急救、作燃料切割金属等 |
| D、氧气从淡蓝色液体变成无色气体发生了化学变化 |
密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
下列说法正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量(g) | 5.3 | 8.4 | 1.0 | 2.4 |
| 反应后质量(g) | 10.6 | 0 | 1.9 | 待测 |
| A、该反应为化合反应 |
| B、反应后生成D的质量为4.6g |
| C、反应过程中,物质C与物质D变化的质量比为9:22 |
| D、若物质A与物质B相对分子质量之比为53:42,反应中A与B的化学计量数之比为1:1 |
 ,下列原子中,与镁原子化学性质相似的原子是
,下列原子中,与镁原子化学性质相似的原子是
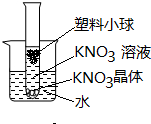 如图所示,烧杯中盛有一定量的水,试管中盛有一定量的有少量固体存在的硝酸钾溶液,在溶液中悬浮着一只塑料小球,请回答下面问题.
如图所示,烧杯中盛有一定量的水,试管中盛有一定量的有少量固体存在的硝酸钾溶液,在溶液中悬浮着一只塑料小球,请回答下面问题.