题目内容
某无色气体可能含有CH4、H2、CO中的一种或几种,将该气体置于充满足量氧气的密闭容器中充分燃烧后,反应结束后测得容器中水和二氧化碳的质量比为9:11,则下列推断错误的是( )
| A、原无色气体可能是纯净的甲烷 |
| B、原无色气体可能是甲烷和氢气的混合气 |
| C、原无色气体可能是一氧化碳和氢气的混合气 |
| D、原气体中一定含有碳元素和氢元素 |
考点:常见气体的检验与除杂方法,质量守恒定律及其应用
专题:物质的检验、鉴别与推断
分析:根据题意,燃烧既生成了水又生成了二氧化碳,结合可燃物完全燃烧的规律,可判断混合气体中含C、H元素;而利用水、二氧化碳的质量进一步确定混合气体中C、H元素的质量比,对于判断混合气体的组成有决定性作用.
解答:解:反应结束后测得容器中水和二氧化碳的质量比为9:11,水中氢元素占:
,二氧化碳中碳元素占:
,所以生成物中碳元素和氢元素的质量比是:(11×
):(9×
)=3:1.
甲烷气体中C、H元素质量比=12:(1×4)=3:1,则混合气体中C、H元素质量比是3:1,因此可判断混合气体可能只有甲烷;也可能只含有CO和H2;也可能是甲烷、氢气、一氧化碳同时存在,不可能含有甲烷和另外任何一种气体.
A、原无色气体可能是纯净的甲烷,是正确的;
B、原无色气体可能是甲烷和氢气的混合气,是错误的;
C、原无色气体可能是一氧化碳和氢气的混合气,是正确的;
D、原气体中一定含有碳元素和氢元素,是正确的.
故选B.
| 2 |
| 18 |
| 12 |
| 44 |
| 12 |
| 44 |
| 2 |
| 18 |
甲烷气体中C、H元素质量比=12:(1×4)=3:1,则混合气体中C、H元素质量比是3:1,因此可判断混合气体可能只有甲烷;也可能只含有CO和H2;也可能是甲烷、氢气、一氧化碳同时存在,不可能含有甲烷和另外任何一种气体.
A、原无色气体可能是纯净的甲烷,是正确的;
B、原无色气体可能是甲烷和氢气的混合气,是错误的;
C、原无色气体可能是一氧化碳和氢气的混合气,是正确的;
D、原气体中一定含有碳元素和氢元素,是正确的.
故选B.
点评:可燃物完全燃烧时,可燃物中的碳元素全部生成二氧化碳,可燃物中的氢元素全部生成水;可燃物完全燃烧生成二氧化碳和水,可判断可燃物中一定含C、H元素.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列物质中,属于碱的是( )
| A、NaCl |
| B、MnO2 |
| C、NaOH |
| D、H2SO4 |
 中国梦?小康梦.我市新农村建设如火如荼,一些村庄道路两侧安装了太阳能路灯,关于太阳能路灯所用材料的叙述不正确的是( )
中国梦?小康梦.我市新农村建设如火如荼,一些村庄道路两侧安装了太阳能路灯,关于太阳能路灯所用材料的叙述不正确的是( )| A、灯泡中填充氮气做保护气 |
| B、氮气可通过分离液态空气得到,此过程是物理变化 |
| C、硅电池板中的硅元素是地壳中含量最多的非金属元素 |
D、硅原子的结构示意图为: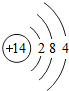 |
由于森林的过量砍伐,草场大面积开垦,土地出现沙漠化,导致我市今天出现了近几年来最严重的沙尘暴天气,使空气中增加了大量的( )
| A、可吸入颗粒 | B、一氧化碳 |
| C、二氧化碳 | D、二氧化硫 |
下列混合物可采用溶解、过滤、蒸发的方法分离的是( )
| A、KCl和MnO2固体 |
| B、NaCl(少量)和KNO3固体 |
| C、Cu和CaCO3粉末 |
| D、Fe和CuSO4粉末 |
除去下列物质中的少量杂质,所用试剂(括号内的物质)不正确的是( )
| A、氮气中的氧气 (铜) |
| B、二氧化碳气体中的水蒸气 (浓硫酸) |
| C、氯化钠溶液中的碳酸钠 (硫酸) |
| D、碳酸钙中的氯化钠 (水) |
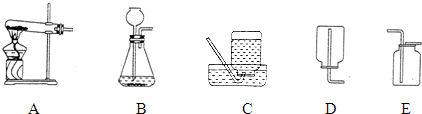
 某同学为研究可燃物的燃烧条件,他查阅资料得知:白磷着火点为40.C,红磷着火点为240.C,它们在空气中燃烧都会生成刺激呼吸道的白烟-五氧化二磷,五氧化二磷易溶于水,并能与水反应.他按如图所示装置进行对比实验.
某同学为研究可燃物的燃烧条件,他查阅资料得知:白磷着火点为40.C,红磷着火点为240.C,它们在空气中燃烧都会生成刺激呼吸道的白烟-五氧化二磷,五氧化二磷易溶于水,并能与水反应.他按如图所示装置进行对比实验.