题目内容
生锈的铁钉放入足量的稀盐酸中,你观察到的现象有 、 .其反应的化学方程式为: 、 .
考点:酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:根据铁锈的主要成分是氧化铁,能与稀盐酸反应生成氯化铁与水,铁锈完全消失后,铁与稀盐酸反应生成氯化亚铁和氢气,会看到铁钉表面有气泡产生,依据物质之间的反应找出反应物、生成物,然后根据质量守恒定律书写化学方程式.
解答:解:铁锈的主要成分是氧化铁(Fe2O3),将生锈的铁钉放入稀盐酸中,先是表面的铁锈的主要成分氧化铁与盐酸反应生成氯化铁与水,反应现象为:铁锈逐渐消失,无色溶液变成黄色,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O,当铁锈完全反应后,铁与稀盐酸发生反应,生成氯化亚铁与氢气,反应现象是有气泡产生,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:铁锈逐渐消失,无色溶液变成黄色、一段时间后,又有气泡产生;Fe2O3+6HCl═2FeCl3+3H2O,Fe+2HCl═FeCl2+H2↑.
故答案为:铁锈逐渐消失,无色溶液变成黄色、一段时间后,又有气泡产生;Fe2O3+6HCl═2FeCl3+3H2O,Fe+2HCl═FeCl2+H2↑.
点评:本题难度不大,主要考查酸的化学性质,掌握铁锈的主要成分、酸的化学性质、化学方程式的书写等是正确解答本题的关键.

练习册系列答案
相关题目
通过两个月的化学学习,你认为化学学科不涉及的研究领域是( )
| A、合成新物质 |
| B、物体的运动形式 |
| C、治理环境污染 |
| D、寻找新能源 |
下例图示操作中,正确的是( )
A、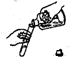 倾倒液体 |
B、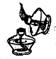 点燃酒精灯 |
C、 用滴管滴加试液 |
D、 给液体加热 |
向量筒内注入水,初次视线与凹液面的最低处相平时读数为a毫升,倒出部分水以后,俯视读数为b毫升,则测出水的体积为( )
| A、(a-b)mL |
| B、大于(a-b)mL |
| C、小于(a-b)mL |
| D、无法确定 |