题目内容
水是生命之源,人类的日常生活与工农业生产都离不开水.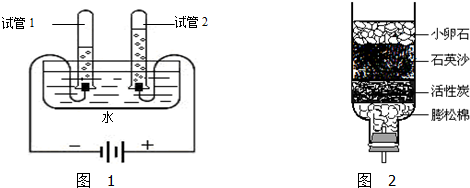
(1)小刚探究水的组成(装置如图1所示).通电一段时间后,试管1中所收集的气体为 ,该实验说明水是由 组成的.通电分解水的文字(或符号)表达式为
(2)小刚要净化收集的雨水,自制了一个简易净水器(如图2所示),其中活性炭和小卵石、石英沙和膨松棉的作用分别是 .
(3)如何检验软水和硬水 .

(1)小刚探究水的组成(装置如图1所示).通电一段时间后,试管1中所收集的气体为
(2)小刚要净化收集的雨水,自制了一个简易净水器(如图2所示),其中活性炭和小卵石、石英沙和膨松棉的作用分别是
(3)如何检验软水和硬水
考点:电解水实验,水的净化,硬水与软水,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:(1)电解水时,与正极相连的玻璃管内产生氧气,与负极相连的玻璃管内产生氢气,且氢气和氧气的体积比为2:1,该实验证明了水是由氢元素和氧元素组成的;
(2)根据水中所含有的杂质,水净化的方式依次是沉降、过滤、消毒、蒸馏等,最后得到的水是蒸馏水;
(3)根据利用肥皂水可区分软硬水进行解答.
(2)根据水中所含有的杂质,水净化的方式依次是沉降、过滤、消毒、蒸馏等,最后得到的水是蒸馏水;
(3)根据利用肥皂水可区分软硬水进行解答.
解答:解:(1)电解水是正极是氧气负极是氢气,由产物可知水是由氢元素和氧元素组成;
(2)在净化雨水时,我们用小卵石、石英沙和膨松棉过滤除去水中的不溶物;
(3)鉴别硬水和软水的方法:分别用两只烧杯取等量水样.向两只烧杯中分别滴加等量肥皂水.泡沫多、浮渣少的为软水.反之,泡沫少、浮渣多的为硬水.
故答案为:(1)氢气;氢元素和氧元素;2H2O
2H2↑+O2↑;
(2)过滤
(3)用肥皂水来检验,泡沫多的为软水,泡沫少的为硬水.
(2)在净化雨水时,我们用小卵石、石英沙和膨松棉过滤除去水中的不溶物;
(3)鉴别硬水和软水的方法:分别用两只烧杯取等量水样.向两只烧杯中分别滴加等量肥皂水.泡沫多、浮渣少的为软水.反之,泡沫少、浮渣多的为硬水.
故答案为:(1)氢气;氢元素和氧元素;2H2O
| ||
(2)过滤
(3)用肥皂水来检验,泡沫多的为软水,泡沫少的为硬水.
点评:对知识的归纳、整理是有效的学习方法,通过对相关知识的归纳、整理可以有效地把零散知识系统化,有利于对类似问题的解答.

练习册系列答案
相关题目
下列各组物质中,都属于混合物的是( )
| A、海水、水银 |
| B、自来水、食盐水 |
| C、空气、冰 |
| D、氮气、氧化铁 |
 铝合金门窗是广泛使用的建筑用品.
铝合金门窗是广泛使用的建筑用品.