题目内容
应用守恒思想解决相关问题,推论正确的是
A.50 mL酒精中加入50 mL水,根据溶质守恒推出酒精溶液的溶质质量分数为50%
B.聚乙烯燃烧生成二氧化碳和水,根据元素守恒推出聚乙烯一定由碳、氢、氧元素组成
C.1mol硫与1mol氧气充分反应,根据质量守恒推出生成二氧化硫的物质的量为2mol
D.酒精燃烧生成CO2和H2O分子个数比为2:3,根据原子守恒推出酒精分子中C、H原子个数比为1:3
D

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验。已知:白磷的着火点为40℃。
| 内容 | ||
| 步骤 | 【实验1】研究燃烧条件 | 【实验2】研究氧气性质 |
| Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2溶液 | 推入适量H2O2溶液 |

(1)H2O2稀溶液与MnO2接触时发生反应的化学方程式为___。
(2)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是_ __; 推入H2O2溶液后,观察到烧杯中的现象是__。
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是__ __;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶。该实验中,集气瓶内压强的变化过程是__ __。
下列除去混合物中少量杂质(括号内为杂质)的方法中,不合理的是( )
| 混合物 | 思路方法 | 选用物质 |
| A.CO(CO2) | 洗气、干燥 | 过量的氢氧化钠溶液、浓硫酸 |
| B.CaCl2(盐酸) | 转化 | 过量的氢氧化钙溶液 |
| C.盐酸(BaCl2) | 沉淀、过滤 | 过量的硫酸铜溶液 |
| D.FeSO4(CuSO4) | 置换、过滤 | 过量的铁粉 |
我国第四套人民币硬币中含有金属镍(Ni),金属镍投入稀盐酸中可看到冒气泡.下列关于金属镍的叙述正确的是( )
|
| A. | 镍在与稀盐酸反应前后化合价不变 |
|
| B. | 金属镍一定能与氯化镁溶液反应 |
|
| C. | 金属镍能与硫酸铜溶液发生置换反应 |
|
| D. | 金属镍在潮湿的空气中容易完全锈蚀 |
 水是宝贵的自然资源,对于人类生活、工农业生产都具有重要意义。
水是宝贵的自然资源,对于人类生活、工农业生产都具有重要意义。 (12) 。(选填编号)
(12) 。(选填编号) 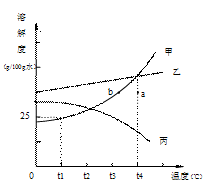 Ⅱ.先锋Ⅵ是一种抗生素,每瓶含先锋霉素0.5g。注射时,配成质量分数不高于20%的溶液,则加入的水至少需要 (13) mL。
Ⅱ.先锋Ⅵ是一种抗生素,每瓶含先锋霉素0.5g。注射时,配成质量分数不高于20%的溶液,则加入的水至少需要 (13) mL。 B.增大与可燃物接触面积 C.与空气中气体反应生成CO2
B.增大与可燃物接触面积 C.与空气中气体反应生成CO2