题目内容
19.把4.5g镁和铝的合金加入到一定质量,一定质量分数的稀盐酸中,恰好完全反应,产生0.4g氢气.向反应后的溶液中加入一定质量的NaOH溶液,恰好使上述产生的MgCl2和AlCl3完全转化为沉淀.则生成NaCl的质量为( )| A. | 23.4g | B. | 29.25g | C. | 11.7g | D. | 5.85g |
分析 根据题意可知,生成的氯化钠中的氯元素全部来自于与4.5g合金反应所消耗的盐酸,因此,计算出所消耗盐酸中的氯元素质量即为最终生成氯化钠中氯元素质量,再利用氯化钠中氯元素的质量分数,即可计算出最终生成氯化钠的质量.
解答 解:方法一:与4.5g镁铝合金反应的盐酸的质量=0.4g÷($\frac{1}{36.5}$×100%)=14.6g
14.6gHCl中Cl元素的质量=14.6g×($\frac{35.5}{36.5}$×100%)=14.2g
含14.2gCl的NaCl的质量=14.2g÷($\frac{35.5}{58.5}$×100%)=23.4g
故选A.
方法一:根据H----HCl---NaCl,则设生成NaCl的质量为x.
1 58.5
0.4g x
则$\frac{1}{58.5}=\frac{0.4g}{x}$,解得x=23.4g
答:生成NaCl的质量为23.4g.
点评 解决本题的技巧在于发现最终生成的氯化钠中氯元素全部来自于与镁铝合金发生反应的盐酸,这样就把看似无法解决的化学方程式的计算转变为根据化学式的计算,从而巧妙地解决问题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列图象能正确反映对应变化关系的是( )
| A. | 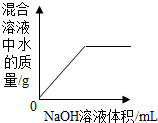 向一定量稀硫酸中加入NaOH溶液 向一定量稀硫酸中加入NaOH溶液 | |
| B. | 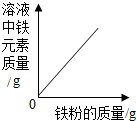 向一定量稀盐酸中加入铁粉 向一定量稀盐酸中加入铁粉 | |
| C. | 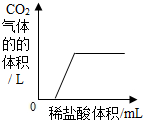 向一定量CaCl2、CaCO3固体混合物中加入稀盐酸 向一定量CaCl2、CaCO3固体混合物中加入稀盐酸 | |
| D. | 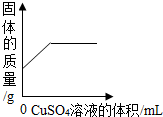 向一定量铁粉中加入CuSO4溶液 向一定量铁粉中加入CuSO4溶液 |
14.下列关于二氧化碳与一氧化碳的比较,错误的是( )
| A. | 组成:都是由碳元素和氧元素组成 | |
| B. | 性质:二氧化碳能溶于水;一氧化碳难溶于水 | |
| C. | 用途:二氧化碳可用作气体肥料;一氧化碳可用作气体燃料 | |
| D. | 危害:二氧化碳会导致“温室效应”增强;一氧化碳会形成酸雨 |
4.物质的性质在很大程度上决定了物质的用途,熟知物质的性质才能更好的应用物质,如图为初中化学教材中的实验.请回答问题:
若按照研究物质性质的角度进行分类,应将实验C归为:
(1)B组(填“A”或“B”),理由是(2)都是研究物质的化学性质;
(3)物质的命名总有一些规律可循.如:含有氧元素的酸一般按照除氢、氧元素以外的元素读作“某酸”,如:“HClO3”读作“氯酸”,“H2CO3”读作“碳酸”.不含氧元素的酸一般按照从左至右的顺序读作“氢某酸”,如H2S读作“氢硫酸”,HI读作“氢碘酸”.按照以上命名方法“HCl”应读作氢氯酸,“磷酸”化学式为H3PO4.
| A组 | B组 | 实验C | ||
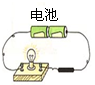 石墨导电实验 | 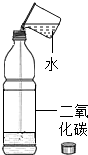 二氧化碳的溶解性实验 | 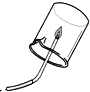 氢气的燃烧 | 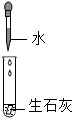 生石灰中加入水 |  酸和碱的溶液改变花的颜色 |
(1)B组(填“A”或“B”),理由是(2)都是研究物质的化学性质;
(3)物质的命名总有一些规律可循.如:含有氧元素的酸一般按照除氢、氧元素以外的元素读作“某酸”,如:“HClO3”读作“氯酸”,“H2CO3”读作“碳酸”.不含氧元素的酸一般按照从左至右的顺序读作“氢某酸”,如H2S读作“氢硫酸”,HI读作“氢碘酸”.按照以上命名方法“HCl”应读作氢氯酸,“磷酸”化学式为H3PO4.
11.下列变化属于物理变化的是( )
| A. | 食物腐败 | B. | 铁钢生锈 | C. | 蜡烛燃烧 | D. | 玻璃破碎 |
8.今有四种粒子的结构示意图,下列说法错误的是( )
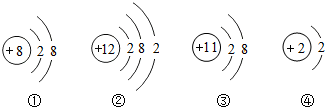

| A. | 它们表示四种元素 | |
| B. | ②表示的元素在化合物中通常显+2价 | |
| C. | ①③④都表示稳定结构 | |
| D. | ①属于离子,离子符号为O2+ |
9.如图所示的实验操作正确的是( )
| A. | 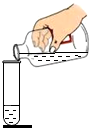 倾倒液体 | B. | 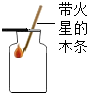 氧气的验满 | C. | 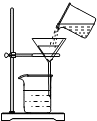 过滤 | D. | 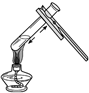 加热液体 |
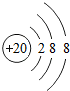 在元素周期表中,元素的周期数与原子核外的电子层数相同.如图是某元素的粒子结构示意图,则该元素的周期数为( )
在元素周期表中,元素的周期数与原子核外的电子层数相同.如图是某元素的粒子结构示意图,则该元素的周期数为( ) 如图是某试剂瓶标签的部分内容.
如图是某试剂瓶标签的部分内容.