题目内容
某同学为了检验家里购买的硫酸铵化肥是否合格,他称取27.5 g化肥样品与足量浓烧碱溶液加热,产生的氨气用100.0g废硫酸吸收。测得吸收氨气的溶液总质量m与反应时间t的变化如右下图所示。所涉及的反应为:
(NH4)2SO4+2NaOH===Na2SO4+2H2O+2NH3↑; 2NH3+H2SO4 == (NH4)2SO4 。
 请计算:
请计算:
(1)完全反应后产生氨气 g。
(2)该化肥的含氮量为 (精确到0.1%),
则这种化肥属于 (填:“合格”或“不合格”。合格硫酸铵含氮量为20%以上)产品
(3)请计算废硫酸中硫酸的质量 分数(写出计算过程)。
分数(写出计算过程)。
(1)6.8g (2)20.4% 合格
(3)解:设废硫酸中纯硫酸的质量为x 。
2NH3 + H2SO4 == (NH4)2SO4,
34 98
6.8g x
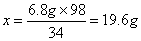
废硫酸中硫酸的质量分数为:(19.6g÷100.0g)×100%=19.6%
答:废硫酸中硫酸的质量分数为19.6%。
解题思路:(1)查图可知完全反应后产生氨气的质量为106.8g-100g= 6.8g
(2)该化肥的含氮量为6.8×14/17 /27.5 ×100% = 20.4% >20%
(3)根据6.8g氨气,通过化学方程式的计算便可算出废硫酸中硫酸的质量分数

 通城学典默写能手系列答案
通城学典默写能手系列答案现有下列仪器或装置,请回答下列问题:

(1)仪器①的名称 ;加热高锰酸钾制取氧气应选装置 (填字母),反应原理的化学方程式为__________________________________,收集O2应采取 法。
|
(2)草酸(H2C2O4) 固体在浓硫酸作用下发生反应: H2C2O4 ====== CO2↑+CO↑+H2O,若用该反应来制取CO,制气装置应选 (填字母);除去其中的CO2可选仪器AC,C中装入的试剂最好是 (填小写字母): a. 烧碱溶液 b. 浓硫酸 c. 澄清石灰水。
 (3)点然CO前应进行的操作是 ;若用CO还原氧化铜粉末,应选装置 (填字母),其反应方程式为 。
(3)点然CO前应进行的操作是 ;若用CO还原氧化铜粉末,应选装置 (填字母),其反应方程式为 。
(4)右图为某种“微型”实验装置。
如果G处装稀盐酸,H处放少量铁屑,
则加热处的现象为 ;
“微型塑料滴管”相当于上图实验装置中
的 (填字母);用微型仪器进行实验,
除试剂用量极少以外,还可能具有的优点是
下列A ~ C是初中化学的三个实验装置,请按要求填空:
 |
(1)A实验中烧杯③的作用是 。
(2)对于B实验,下列操作不正确的是 。(填序号)
①红磷要足量 ②实验前夹紧止水夹 ③冷却后再打开止水夹 ④用木炭代替红磷
(3)C实验中,气球的变化情况是 。写出导致气球膨胀的反应的化学方程式 。
 )
)