题目内容
 如图是一定体积的氢气和不同体积的氧气化合成水(液态)的实验数据的关系图(横坐标表示反应前氧气的体积,纵坐标表示反应后剩余气体的体积,气体体积均在同温同压下测定).试回答:
如图是一定体积的氢气和不同体积的氧气化合成水(液态)的实验数据的关系图(横坐标表示反应前氧气的体积,纵坐标表示反应后剩余气体的体积,气体体积均在同温同压下测定).试回答:(1)实线部分表示剩余的气体是
(2)虚线部分表示剩余的气体是
(3)实线与虚线的交点表示的意义是
(4)写出该反应的化学方程式:
分析:根据化学方程式来考虑参加反应的氢气与氧气两者之间的关系来进行判断.从氢气与氧气反应的方程式:2H2+O2
2H2O,可以看出:消耗的氢气与氧气的体积比2:1.
| ||
解答:解:反应的方程式为:2H2+O2
2H2O,从图中可以看出:每增加1mL的氧气,氢气则减少2mL,当氧气体积小于3mL时,氢气有剩余;当氧气体积为3ml时,两者完全反应;氧气大于3mL时,氢气被反应有氧气剩余.故实线部分表示有氢气剩余;实线与虚线的交点(坐标为3,0)为两者恰好完全反应;虚线部分表示氧气剩余.
氢气燃烧生成了水,该反应的化学方程式:2H2+O2
2H2O.
故答案为:(1)氢气;(2)氧气;(3)氧气为3mL时,氧气与氢气恰好完全反应生成水,剩余气体的体积为0.(4)2H2+O2
2H2O.
| ||
氢气燃烧生成了水,该反应的化学方程式:2H2+O2
| ||
故答案为:(1)氢气;(2)氧气;(3)氧气为3mL时,氧气与氢气恰好完全反应生成水,剩余气体的体积为0.(4)2H2+O2
| ||
点评:根据图象所表明的反应物中氢气与氧气的体积关系,围绕图象表明变化关系得出结论.

练习册系列答案
相关题目
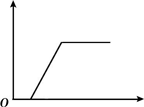 25、下表中的选项符合如图所示曲线的是( )
25、下表中的选项符合如图所示曲线的是( )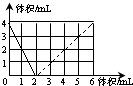 如图是一定体积的氢气和不同体积的氧气化合成水(液态)的实验数据的关系图(横坐标表示通入氧气的体积,纵坐标表示反应后剩余的气体的体积,气体体积均在同温同压下测定),下列说法错误的是( )
如图是一定体积的氢气和不同体积的氧气化合成水(液态)的实验数据的关系图(横坐标表示通入氧气的体积,纵坐标表示反应后剩余的气体的体积,气体体积均在同温同压下测定),下列说法错误的是( )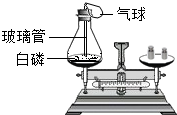
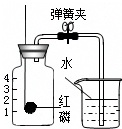 空气不仅是人类和一切动植物生命的支柱,而且也是人类生产活动的重要自然资源.
空气不仅是人类和一切动植物生命的支柱,而且也是人类生产活动的重要自然资源.