题目内容
结合图1、图2所示实验装置回答问题:

(1)实验室若用高锰酸钾制取氧气,可选用的发生和收集装置是 (填标号)
(2)检查装置B气密性的方法是 .
(3)装置B与C组合,可以制取的一种气体是 ,反应的化学方程式为 ,能用装置C收集该气体的原因是 .
(4)一种洗气装置如图2所示,为了除去二氧化碳中混有的少量水分,气体应从 (填“a”或“b”)端导管口通入.

(1)实验室若用高锰酸钾制取氧气,可选用的发生和收集装置是
(2)检查装置B气密性的方法是
(3)装置B与C组合,可以制取的一种气体是
(4)一种洗气装置如图2所示,为了除去二氧化碳中混有的少量水分,气体应从
考点:常用气体的发生装置和收集装置与选取方法,检查装置的气密性,气体的干燥(除水),实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据反应物的状态和反应条件选择发生装置,根据氧气的水溶性和密度选择收集装置;
(2)据装置特点和检查装置气密性的方法分析解答;
(3)装置B是适合固液反应,不用加热或液液反应不用加热的制气反应,C装置收集密度比空气大的气体,并结合实验室制取氧气、二氧化碳和氢气的方法分析解答,
(4)洗气装置中导管长进短出.
(2)据装置特点和检查装置气密性的方法分析解答;
(3)装置B是适合固液反应,不用加热或液液反应不用加热的制气反应,C装置收集密度比空气大的气体,并结合实验室制取氧气、二氧化碳和氢气的方法分析解答,
(4)洗气装置中导管长进短出.
解答:解:(1)高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应属于固体加热制气,可选用发生装置A,
氧气是不溶于水的,所以可以选用排水收集,装置为E;氧气密度大于空气,所以可以选择向上排空气法收集,装置为C,故发生和收集装置是AC或AE;
(2)检查装置B气密性的方法是:先从长颈漏斗中注入水,当水浸没其下端管口时,用弹簧夹,夹住导气管上连接的胶皮管,然后再加入少量的水,若停止加水后,长颈漏斗中的水面不再下降,则说明此装置气密性良好;
(3)B装置是适合固液不加热制气或液液不加热制气,C为向上排空气法,收集的气体密度要比空气大,
实验室用大理石和盐酸反应制备二氧化碳,不需加热,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;实验室用双氧水分解制取氧气也可用此套装置;
(4)为了除去二氧化碳中混有的少量水分,用浓硫酸,导管长进短出,所以应从a端进气;
故答案为:(1)AC或AE;
(2)先从长颈漏斗中注入水,当水浸没其下端管口时,用弹簧夹,夹住导气管上连接的胶皮管,然后再加入少量的水,若停止加水后,长颈漏斗中的水面不再下降,则说明此装置气密性良好;
(3)二氧化碳(合理均可);CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳的密度比空气大;
(4)a.
氧气是不溶于水的,所以可以选用排水收集,装置为E;氧气密度大于空气,所以可以选择向上排空气法收集,装置为C,故发生和收集装置是AC或AE;
(2)检查装置B气密性的方法是:先从长颈漏斗中注入水,当水浸没其下端管口时,用弹簧夹,夹住导气管上连接的胶皮管,然后再加入少量的水,若停止加水后,长颈漏斗中的水面不再下降,则说明此装置气密性良好;
(3)B装置是适合固液不加热制气或液液不加热制气,C为向上排空气法,收集的气体密度要比空气大,
实验室用大理石和盐酸反应制备二氧化碳,不需加热,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;实验室用双氧水分解制取氧气也可用此套装置;
(4)为了除去二氧化碳中混有的少量水分,用浓硫酸,导管长进短出,所以应从a端进气;
故答案为:(1)AC或AE;
(2)先从长颈漏斗中注入水,当水浸没其下端管口时,用弹簧夹,夹住导气管上连接的胶皮管,然后再加入少量的水,若停止加水后,长颈漏斗中的水面不再下降,则说明此装置气密性良好;
(3)二氧化碳(合理均可);CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳的密度比空气大;
(4)a.
点评:本题主要对气体的制备的反应原理、发生装置、气体的收集装置的选择进行考查.平时同学们要对实验室制气中氧气、二氧化碳和氢气的制备进行比较、归纳.

练习册系列答案
相关题目
下例物质中一定属于混合物的是( )
| A、含多种元素的物质 |
| B、含多种分子的物质 |
| C、含多种原子的物质 |
| D、只含有一种元素的物质 |
 某化学兴趣小组用如图所示装置做有关二氧化碳气体性质的实验:
某化学兴趣小组用如图所示装置做有关二氧化碳气体性质的实验: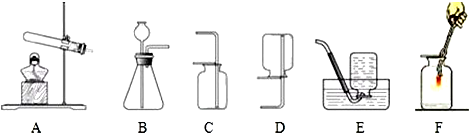
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.