题目内容
 让我们与小松同学一起参与以下探究:
让我们与小松同学一起参与以下探究:(1)Cu-Al和Cu-Ag合金外观相似,小松认为只要滴几滴稀硫酸就可将这两种合金鉴别出来.你是否同意小松的看法?
(2)小松认为分别加稀硫酸,就可测定上述
| 样 品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
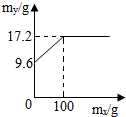
(3)小松认为只使用AgNO3溶液,就可测定上述合金中两种 金属的质量比,还可测出AgNO3溶液的质量分数,于是进行了多次实验,记录了每次使用的AgNO3溶液质量mx和充分反应后所得固体质量my,并绘制了如图,则 AgNO3溶液的溶质质量分数是
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)因为 Cu Ag不与盐酸反应,Al能与盐酸反应,所以滴加盐酸后CU-AL合金会与盐酸反应.
(2)首先对合金的类型进行判断,再利用物质反应时量的关系进行分析探讨解决,首先利用方程式铝与氢气的关系即可计算铝的质量,即可求出质量比.
(3)分析图象知完全反应时硝酸银溶液的质量是100g,利用化学方程式中固体质量差求出硝酸银溶液溶质质量分数求解即可.
(2)首先对合金的类型进行判断,再利用物质反应时量的关系进行分析探讨解决,首先利用方程式铝与氢气的关系即可计算铝的质量,即可求出质量比.
(3)分析图象知完全反应时硝酸银溶液的质量是100g,利用化学方程式中固体质量差求出硝酸银溶液溶质质量分数求解即可.
解答:解:(1)因为 Cu Ag不与盐酸反应,Al能与盐酸反应,所以滴加盐酸后Cu-Al合金会与盐酸反应.故答案:同意;
(2)设,Cu-Al合金中铝的质量为x,
2Al+6HCl=2AlCl3+3H2↑
54 6
x 1.0g
=
x=9g
样品中两种金属的质量比:Cu:Al=(50g-9g):9g=41:9
答:样品中铜与铝的质量比是41:9.
(3)设硝酸银的溶质质量分数是w%
则有 Cu+2AgNO3 =Cu(NO3)2 +2Ag 固体重量增加
64 340 216 216-64=152
100g?w% 17.2g-9.6g=7.6g
=
w%=17%
答:硝酸银的溶质质量分数是硝酸银的溶质质量分数是
(2)设,Cu-Al合金中铝的质量为x,
2Al+6HCl=2AlCl3+3H2↑
54 6
x 1.0g
| 54 |
| x |
| 6 |
| 1.0g |
x=9g
样品中两种金属的质量比:Cu:Al=(50g-9g):9g=41:9
答:样品中铜与铝的质量比是41:9.
(3)设硝酸银的溶质质量分数是w%
则有 Cu+2AgNO3 =Cu(NO3)2 +2Ag 固体重量增加
64 340 216 216-64=152
100g?w% 17.2g-9.6g=7.6g
| 340 |
| 100g?w% |
| 152 |
| 7.6g |
w%=17%
答:硝酸银的溶质质量分数是硝酸银的溶质质量分数是
点评:此题属一道综合计算题,涉及到化学方程式及溶液的计算,解题的关键是对问题进行深入的探讨与分析,从而确定反应时量的关系,从难度上讲应该属于竞赛题系列.

练习册系列答案
相关题目
分别将下列各组物质同时加入水中,能得到无色透明溶液的是( )
| A、HCl、Na2SO4、KCl |
| B、MgCl2、HNO3、AgNO3 |
| C、NaCl、BaCO3、KNO3 |
| D、CuSO4、KOH、NaCl |
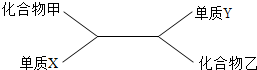 根据下列化合物与单质相互转化的关系回答:
根据下列化合物与单质相互转化的关系回答: