题目内容
实验室用铁、氧化铜、稀硫酸为原料制取铜,某同学设计了两个实验方案:方案一:Fe
 H2
H2 Cu
Cu方案二:CuO
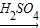 CuSO4
CuSO4 Cu
Cu(1)写出上述两个方案每步转化的化学方程式.
方案一 , ;
方案二 , .
(2)两个实验方案中,最好的是 ,理由是 .
(3)由以上两个生成相同质量的铜,则铁、氧化铜、稀硫酸三种原料中,消耗量相同的是 ,理由是 .
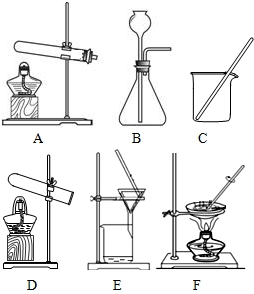
(4)方案一应选用下图中的(填序号) 装置.对于这种方法制取的铜中可能含有的杂质可加 除去.

【答案】分析:(1)化学方程式的书写要注意以下三点:①正确写出反应物和生成物的化学式,②正确的配平化学方程式,③注明反应条件和生成物状态.
(2)判断一个实验方案的好坏要从操作简便,结果明显,环保,节能等角度考虑.
(3)可以根据质量守恒定律来判断反应前后某些物质的质量.
(4)选择实验装置时要根据反应物的状态和反应条件.
解答:解:(1)方案一是用铁和酸反应制取氢气,再用氢气还原氧化铜,化学方程式为:Fe+H2SO4=FeSO4+H2↑,H2+CuO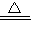 Cu+H2O;
Cu+H2O;
方案二是用氧化铜与酸反应得到铜盐溶液,再用铁置换出铜,化学方程式为:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4.
(2)方案二不需加热,操作方便安全,且节省原料,所以比方案一要优越.
(3)方案一中由于所用的氢气要过量,所以要消耗的铁和稀硫酸比方案二多,根据质量守恒定律,氧化铜中的铜元素全部生成了单质铜,且反应中氧化铜无损失.
(4)方案一要先制取氢气,然后用氢气还原热的氧化铜,所以装置应选择BD,没有完全反应的氧化铜可以稀硫酸除去.
故答案为:(1)方案一:Fe+H2SO4=FeSO4+H2↑,H2+CuO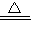 Cu+H2O;
Cu+H2O;
方案二:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4.
(2)方案二,不需加热,操作方便安全,且节省原料.
(3)氧化铜根据质量守恒定律,氧化铜中的铜元素全部生成了单质铜,且反应中氧化铜无损失.
(4)B,D,稀硫酸
点评:本题从化学方程式,实验方案的评价,实验装置是选择等方面进行考查,综合性强,是一道很好的中考题.
(2)判断一个实验方案的好坏要从操作简便,结果明显,环保,节能等角度考虑.
(3)可以根据质量守恒定律来判断反应前后某些物质的质量.
(4)选择实验装置时要根据反应物的状态和反应条件.
解答:解:(1)方案一是用铁和酸反应制取氢气,再用氢气还原氧化铜,化学方程式为:Fe+H2SO4=FeSO4+H2↑,H2+CuO
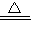 Cu+H2O;
Cu+H2O;方案二是用氧化铜与酸反应得到铜盐溶液,再用铁置换出铜,化学方程式为:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4.
(2)方案二不需加热,操作方便安全,且节省原料,所以比方案一要优越.
(3)方案一中由于所用的氢气要过量,所以要消耗的铁和稀硫酸比方案二多,根据质量守恒定律,氧化铜中的铜元素全部生成了单质铜,且反应中氧化铜无损失.
(4)方案一要先制取氢气,然后用氢气还原热的氧化铜,所以装置应选择BD,没有完全反应的氧化铜可以稀硫酸除去.
故答案为:(1)方案一:Fe+H2SO4=FeSO4+H2↑,H2+CuO
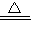 Cu+H2O;
Cu+H2O;方案二:CuO+H2SO4=CuSO4+H2O,CuSO4+Fe=Cu+FeSO4.
(2)方案二,不需加热,操作方便安全,且节省原料.
(3)氧化铜根据质量守恒定律,氧化铜中的铜元素全部生成了单质铜,且反应中氧化铜无损失.
(4)B,D,稀硫酸
点评:本题从化学方程式,实验方案的评价,实验装置是选择等方面进行考查,综合性强,是一道很好的中考题.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目

 H2
H2 Cu
Cu  CuSO4
CuSO4 Cu
Cu 