题目内容
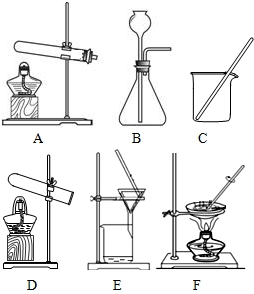
实验室用铁、氧化铜、硫酸为原料制取铜,某同学设计了如右两个实验方案:
认真分析实验方案,回答下列问题:
(1)写出CuSO4溶液和Fe反应的化学方程式 .
(2)两个方案中,你认为较好的是哪一个,请简述理由 .
【答案】分析:(1)化学方程式的书写要注意以下三点:①正确写出反应物和生成物的化学式,②正确的配平化学方程式,③注明反应条件和生成物状态;
(2)判断一个实验方案的好坏要从操作简便,结果明显,环保,节能等角度考虑.
解答:解:(1)用铁和硫酸铜反应生成了硫酸亚铁和铜,化学方程式为:CuSO4+Fe=FeSO4+Cu;
(2)方案二不需加热,操作方便安全,且节省原料,所以比方案一要优越.
故答案为:(1)CuSO4+Fe=FeSO4+Cu;
(2)方案②不需加热;反应物充分利用 节约能源或方案①反应物需要加热 反应物不能充分利用 耗损能源.
点评:本题从化学方程式,实验方案的评价,等方面进行考查,综合性强,是一道很好的中考题.
(2)判断一个实验方案的好坏要从操作简便,结果明显,环保,节能等角度考虑.
解答:解:(1)用铁和硫酸铜反应生成了硫酸亚铁和铜,化学方程式为:CuSO4+Fe=FeSO4+Cu;
(2)方案二不需加热,操作方便安全,且节省原料,所以比方案一要优越.
故答案为:(1)CuSO4+Fe=FeSO4+Cu;
(2)方案②不需加热;反应物充分利用 节约能源或方案①反应物需要加热 反应物不能充分利用 耗损能源.
点评:本题从化学方程式,实验方案的评价,等方面进行考查,综合性强,是一道很好的中考题.

练习册系列答案
相关题目

 H2
H2 Cu
Cu  CuSO4
CuSO4 Cu
Cu