题目内容
将铝丝插入到硫酸铜溶液中,可观察到铝丝表面出现红色固体,溶液由蓝色逐渐变为无色.该反应的化学方程式为 .
【答案】分析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答:解:铝的活动性比铜强,将铝丝插入到硫酸铜溶液中,铝能与硫酸铜反应生成硫酸铝和铜,可观察到铝丝表面出现红色固体,溶液由蓝色逐渐变为无色,反应的化学方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu.
故答案为:2Al+3CuSO4=Al2(SO4)3+3Cu.
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.
解答:解:铝的活动性比铜强,将铝丝插入到硫酸铜溶液中,铝能与硫酸铜反应生成硫酸铝和铜,可观察到铝丝表面出现红色固体,溶液由蓝色逐渐变为无色,反应的化学方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu.
故答案为:2Al+3CuSO4=Al2(SO4)3+3Cu.
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
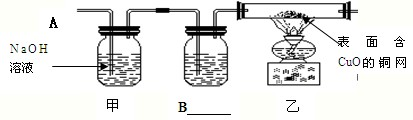
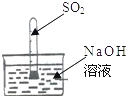 他的理由是
他的理由是