题目内容
实验室中以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成活泼性更强的单质铁.请回答下列问题:(1)写出化学方程式______ Fe+2HCl
【答案】分析:(1)本问属于信息型方程式的书写,题目已经告诉反应物为氢气和氯化亚铁,生成物有单质铁,同时根据质量守恒定律,其余生成物还含有氢元素和氯元素,且是置换反应,所以氢元素和氯元素在同一物质,即为氯化氢.
(2)氮气的保护作用首先是自身的性质的稳定,其次是要考虑怎么防止铁反应,此时要考虑环境中存在的可能与铁反应的物质是什么.
解答:解:(1)在高温条件下用H2和FeCl2发生置换反应,生成活泼性更强的单质铁,反应物为氢气和氯化亚铁,生成物之一为铁,反应为置换反应,根据质量守恒定律可知另外生成物一定是HCl.故化学方程式为:FeCl2+H2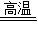 Fe+2HCl.
Fe+2HCl.
(2)氮气在本转化中的保护作用首先是因为氮气的化学性质稳定,不能和氢气等反应物以及铁等生成物反应,同时由于目的是制造活泼性更强的单质铁,所以保护的是铁,此时环境中存在的物质有氢气、氯化亚铁以及HCl,在这些物质中能够与铁反应的只有HCl气体,所以氮气的存在减少或者一定程度上阻止了铁与HCl的接触,进而保证反应顺利进行.故答案为:氮气化学性质稳定在高温下不与铁等物质反应;氮气的存在减少或者一定程度上阻止了铁与HCl的接触,进而保证反应顺利进行.
点评:信息型方程式的书写,关键是提炼信息,从信息中需求问题的答案.
(2)氮气的保护作用首先是自身的性质的稳定,其次是要考虑怎么防止铁反应,此时要考虑环境中存在的可能与铁反应的物质是什么.
解答:解:(1)在高温条件下用H2和FeCl2发生置换反应,生成活泼性更强的单质铁,反应物为氢气和氯化亚铁,生成物之一为铁,反应为置换反应,根据质量守恒定律可知另外生成物一定是HCl.故化学方程式为:FeCl2+H2
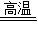 Fe+2HCl.
Fe+2HCl.(2)氮气在本转化中的保护作用首先是因为氮气的化学性质稳定,不能和氢气等反应物以及铁等生成物反应,同时由于目的是制造活泼性更强的单质铁,所以保护的是铁,此时环境中存在的物质有氢气、氯化亚铁以及HCl,在这些物质中能够与铁反应的只有HCl气体,所以氮气的存在减少或者一定程度上阻止了铁与HCl的接触,进而保证反应顺利进行.故答案为:氮气化学性质稳定在高温下不与铁等物质反应;氮气的存在减少或者一定程度上阻止了铁与HCl的接触,进而保证反应顺利进行.
点评:信息型方程式的书写,关键是提炼信息,从信息中需求问题的答案.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目