题目内容
某化学兴趣小组研究制取氢氧化钠溶液.小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”他设计了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量无色溶液于试管中,滴 人2滴无色酚酞试液 | 无色酚酞试液变红色 | 无色溶液中含有氢氧化钠 |
| 实验步骤 | 实验现象 | 实验结论 |
| 无色溶液中确实含有氢氧化钠 |
碳酸钠溶液也能使酚酞溶液变红 排除了碳酸钠的干扰
分析:根据同学的叙述和复分解反应的原理进行分析,根据只要溶液显碱性就会使酚酞变红进行分析,根据两同学实验的中需要考虑的因素进行分析.
解答:根据“小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!””,可以知道该反应是用氢氧化钙和碳酸钠反应制取氢氧化钠的.小丽同学:只要是碱性的溶液就是使无色酚酞变成红色,反应后的溶液中除了氢氧化钠外,也可能有碳酸钠,都显碱性,故答案为:碳酸钠溶液也会使无色酚酞变红色,
实验:加入试剂屏蔽碳酸钠,排除碳酸钠的干扰,将碳酸钠转化为沉淀就行了.取少量样品于试管中,加入氯化钡溶液,过滤,在滤液中滴入无色的酚酞,生成白色沉淀,无色酚酞变红;则说明无色溶液中确实含有氢氧化钠.
小欢和小丽的实验都是为了证实小京实验结论的可靠性,显然小丽的实验可靠性比小欢的实验好,其原因是排除了干扰因素.
故答案为:碳酸钠溶液也能使酚酞溶液变红(或碳酸钠溶液也显碱性)
排除了碳酸钠的干扰.
点评:此类题的起点较高,落点低,阅读量大,实际的解答不难,主要从心理上考查学生的临场能力.
分析:根据同学的叙述和复分解反应的原理进行分析,根据只要溶液显碱性就会使酚酞变红进行分析,根据两同学实验的中需要考虑的因素进行分析.
解答:根据“小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!””,可以知道该反应是用氢氧化钙和碳酸钠反应制取氢氧化钠的.小丽同学:只要是碱性的溶液就是使无色酚酞变成红色,反应后的溶液中除了氢氧化钠外,也可能有碳酸钠,都显碱性,故答案为:碳酸钠溶液也会使无色酚酞变红色,
实验:加入试剂屏蔽碳酸钠,排除碳酸钠的干扰,将碳酸钠转化为沉淀就行了.取少量样品于试管中,加入氯化钡溶液,过滤,在滤液中滴入无色的酚酞,生成白色沉淀,无色酚酞变红;则说明无色溶液中确实含有氢氧化钠.
小欢和小丽的实验都是为了证实小京实验结论的可靠性,显然小丽的实验可靠性比小欢的实验好,其原因是排除了干扰因素.
故答案为:碳酸钠溶液也能使酚酞溶液变红(或碳酸钠溶液也显碱性)
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量无色溶液于试管中,加入足量的氯化钙(或硝酸钙)溶液,过滤,在滤液中滴加无色酚酞溶液 | 生成白色沉淀, 酚酞溶液变红 |
点评:此类题的起点较高,落点低,阅读量大,实际的解答不难,主要从心理上考查学生的临场能力.

练习册系列答案
相关题目
某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
[查阅资料]
<资料1>该厂采用“侯氏制碱法”生产的化工产品为纯碱(化学式为 )和氯化铵.
(“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺.)
<资料2>生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
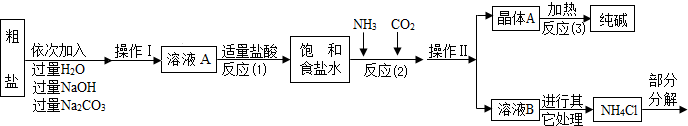
<资料3>部分生产流程如下图所示.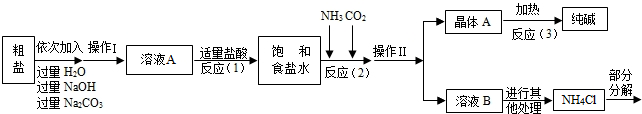
上述流程中涉及的部分反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;
Na2CO3+CaCl2=CaCO3↓+2NaCl;NH4Cl═NH3↑+HCl↑
生产原理:将氨气(NH3)和二氧化碳通入饱和食盐水中得到小苏打和氯化铵的混合物,其反应的化学方程式为:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(晶体)↓+NH4Cl;分离出NaHCO3,使其充分受热即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为 .
【问题讨论】
(1)溶液A中的溶质为 ,操作Ⅱ的名称为 .
(2)上述生产流程中可循环使用的是 (填序号).
A.CO2B.NH3C.HCl D.NaOH E.Na2CO3
(3)根据上述信息,请你设计实验区分碳酸钠和碳酸氢钠.
【含量测定】
同学们为了测定该纯碱样品的纯度,设计了如下实验.
甲组:取10.0g纯碱样品(假定杂质在整个实验过程中不发生变化),向其中加入过量的盐酸,直至样品中无气泡冒出.充分加热蒸发所得物质并干燥、冷却至室温后称量,所得固体质量为10.9g.样品中碳酸钠的质量分数为 (结果保留一位小数).
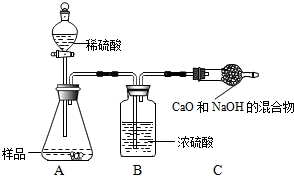
乙组:取10.0g纯碱样品,利用右图所示装置,测出反应后装置C增重了3.5g(所加试剂均足量).
实验结束后,发现乙组测定的质量分数偏小,其原因是 .
[查阅资料]
<资料1>该厂采用“侯氏制碱法”生产的化工产品为纯碱(化学式为
(“侯氏制碱法”是我国近代著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺.)
<资料2>生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质.
<资料3>部分生产流程如下图所示.

上述流程中涉及的部分反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;
Na2CO3+CaCl2=CaCO3↓+2NaCl;NH4Cl═NH3↑+HCl↑
生产原理:将氨气(NH3)和二氧化碳通入饱和食盐水中得到小苏打和氯化铵的混合物,其反应的化学方程式为:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(晶体)↓+NH4Cl;分离出NaHCO3,使其充分受热即可分解制得纯碱及两种常见的氧化物,此反应的化学方程式为
【问题讨论】
(1)溶液A中的溶质为
(2)上述生产流程中可循环使用的是
A.CO2B.NH3C.HCl D.NaOH E.Na2CO3
(3)根据上述信息,请你设计实验区分碳酸钠和碳酸氢钠.
| 实验步骤 | 实验现象 | 实验结论 |
同学们为了测定该纯碱样品的纯度,设计了如下实验.

甲组:取10.0g纯碱样品(假定杂质在整个实验过程中不发生变化),向其中加入过量的盐酸,直至样品中无气泡冒出.充分加热蒸发所得物质并干燥、冷却至室温后称量,所得固体质量为10.9g.样品中碳酸钠的质量分数为
乙组:取10.0g纯碱样品,利用右图所示装置,测出反应后装置C增重了3.5g(所加试剂均足量).
实验结束后,发现乙组测定的质量分数偏小,其原因是