题目内容
向盐酸中加入过量某物质X,溶液的pH随加入X的量的变化关系如右下图所示。则X是
| A.水 |
| B.铜粉 |
| C.氯化钠溶液 |
| D.澄清石灰水 |
D
解析试题分析:根据盐酸的性质结合图像分析。
A.向盐酸中加入过量的水,盐酸会被稀释,酸性减弱,其溶液的pH会变大,但由于溶液始终为酸性,故其最终的pH依然<7,错误;
B.铜不与盐酸反应,且不溶于水,故溶液的pH不变,错误;
C.氯化钠溶液呈中性,故向盐酸中加入过量的氯化钠溶液,同样起到的是稀释作用,故其最终的pH依然<7,错误;
D.澄清石灰水是碱液,能与盐酸发生中和反应,生成盐和水,故溶液的pH会变大,当澄清石灰水过量时,溶液的pH大于7,正确。故选D
考点:酸的化学性质,溶液的酸碱性与pH值的关系
点评:本题是化学反应中定量关系和图象相结合的题型,要准确解答此类题,关键要对化学反应知识熟练,并能结合图象的数学意义,综合考虑;图象的意义要抓住三点:①抓图象的起点,②抓图象的终点,③抓图象的变化过程。

练习册系列答案
相关题目
某同学设计实验,请协助其完成实验报告,并回答相关问题.
(一)实验目的:研究化学反应速率与反应物浓度的关系
(二)实验用品:稀盐酸NaOH溶液铝片红色石蕊试纸蓝色石蕊试纸烧杯玻璃棒胶头滴管
(三)实验内容:
(四)该同学对实验步骤的现象进行如下探究:
(1)查阅资料后得知:铝也能和氢氧化钠溶液反应2Al+2NaOH+2H2O═2NaAlO2+3H2↑为证明第三步操作时,NaOH已经完全过量,该同学可以采用______的操作
(2)若最终铝片完全溶解,则得到的H2比铝片全部与盐酸反应得到的H2质量(______ )
A、偏大;B、相等
C、偏小;D、无法确定.
(一)实验目的:研究化学反应速率与反应物浓度的关系
(二)实验用品:稀盐酸NaOH溶液铝片红色石蕊试纸蓝色石蕊试纸烧杯玻璃棒胶头滴管
(三)实验内容:
| 实验步骤 | 实验现象 | 结论、解释与化学方程式 |
| 1、向一定量的盐酸中加入铝片 | 有_____________出现 | 化学方程式: _____________________ |
| 2、向上述正在反应中的溶液里逐滴加入NaOH溶液 | 产生气泡的速度逐渐减慢;一段时间后,溶液中没有气泡放出. | 原因:_______________ 化学方程式:__________ 结论:_______________ |
| 3、继续向上述溶液中滴加NaOH溶液 | 溶液中又开始有气泡生成 | ------------------ |
(1)查阅资料后得知:铝也能和氢氧化钠溶液反应2Al+2NaOH+2H2O═2NaAlO2+3H2↑为证明第三步操作时,NaOH已经完全过量,该同学可以采用______的操作
(2)若最终铝片完全溶解,则得到的H2比铝片全部与盐酸反应得到的H2质量(______ )
A、偏大;B、相等
C、偏小;D、无法确定.
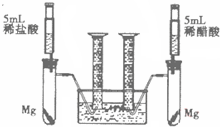 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.
