题目内容
14.回答下列与金属有关的问题.(1)在生铁、钢、铝和黄铜中,不属于合金的是铝;
(2)在空气中金属铝比金属铁更耐腐蚀,原因是金属铝的表面形成了一层致密氧化铝的薄膜;
(3)向AgNO3、Cu(NO3)2、Zn(NO3)2士的混合溶液中加人一定量铁粉,充分反应后过滤.下列关于
所得滤渣和滤液的分析正确的是A.
A、滤渣中一定含有Ag,可能含有Cu、Fe
B、滤渣中一定含有Ag、Cu、Fe,可能含有Zn
C、滤液中一定含有 Zn(NO3)2,可能含有 Fe(NO3)2、AgNO3、Cu(NO3)2
D、滤液中一定含有 Zn(NO3)2、Fe(NO3)2、AgNO3,可能含有Cu(NO3)2.
分析 (1)根据合金的特点分析;
(2)根据铝的特性分析;
(3)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,利用此知识分析即可.
解答 解:(1)在生铁、钢、铝和黄铜中,不属于合金的是铝;
(2)在空气中金属铝比金属铁更耐腐蚀,原因是:金属铝的表面形成了一层致密氧化铝的薄膜;
(3)【解答】在金属活动性顺序中,金属的活动性是:锌>铁>氢>铜>银.向AgNO3、Cu(NO3)2、Zn(NO3)2士的混合溶液中加人一定量铁粉,铁首先与硝酸银反应生成银和硝酸亚铁,当硝酸银反应完全后,再与硝酸铜反应生成铜和硝酸亚铁,不能与硝酸锌反应;
A、当铁粉过量时,滤渣中一定含有Ag,可能含有Cu、Fe,故A正确;
B、由于锌比铁活泼,铁不能将锌置换出来.故B错误;
C、滤液中一定含有 Zn(NO3)2、Fe(NO3)2,可能含有AgNO3、Cu(NO3)2,故C错误;
D、由于铁首先与硝酸银反应生成银和硝酸亚铁,当硝酸银反应完全后,再与硝酸铜反应生成铜和硝酸亚铁,当铁不足量时,滤液中一定含有 Zn(NO3)2、Fe(NO3)2、Cu(NO3)2,可能含有AgNO3,故D错误.
故选项为:(1)铝;(2)金属铝的表面形成了一层致密氧化铝的薄膜;(3)A.
点评 此题考查了金属的性质和金属活动顺序表中锌、铁、铜、银的金属活动性强弱,及其金属活动性顺序表的应用,锻炼了学生分析问题解决问题的能力.

练习册系列答案
相关题目
6.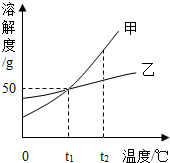 如图为两种固体物质(不含结晶水)的溶解的曲线,下列说法正确的是( )
如图为两种固体物质(不含结晶水)的溶解的曲线,下列说法正确的是( )
 如图为两种固体物质(不含结晶水)的溶解的曲线,下列说法正确的是( )
如图为两种固体物质(不含结晶水)的溶解的曲线,下列说法正确的是( )| A. | 乙的饱和溶液由t2℃降温至t1℃,变为不饱和溶液 | |
| B. | t2℃等质量的甲、乙两种物质的饱和溶液中,溶质的质量一定是甲大于乙 | |
| C. | t1℃甲、乙两种物质的饱和溶液中溶质的质量分数都是50% | |
| D. | 甲溶液中含有少量乙,可用蒸发溶剂的方法提纯甲 |
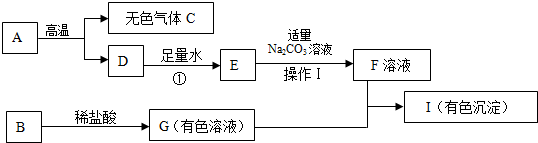
4. 已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热易分解生成碳酸钙和一种有毒的气体;碳酸钙高温分解生成氧化钙和二氧化碳;草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4).相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4
已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热易分解生成碳酸钙和一种有毒的气体;碳酸钙高温分解生成氧化钙和二氧化碳;草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4).相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4
(1)实验一:取一定量草酸钙固体,加热.加热过程中剩余固体的质量随时间变化如图所示.图中AB段发生反应的化学方程式为CaC2O4$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO↑,
DE段固体所含物质为CaO,或氧化钙(写化学式或物质名称均可,下同).
(2)实验二:探究草酸钙加热一段时间后剩余固体M的成分.
(3)若加热前草酸钙的质量为6.4g,加热一段时间后剩余固体的质量为4.8g,则该固体中含有的物
质是碳酸钙和氧化钙.
 已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热易分解生成碳酸钙和一种有毒的气体;碳酸钙高温分解生成氧化钙和二氧化碳;草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4).相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4
已知:草酸钙(CaC2O4)是一种难溶于水的白色固体,受热易分解生成碳酸钙和一种有毒的气体;碳酸钙高温分解生成氧化钙和二氧化碳;草酸钙能与稀盐酸反应生成氯化钙和可溶于水的草酸(H2C2O4).相关反应的化学方程式为:CaC2O4+2HCl═CaCl2+H2C2O4(1)实验一:取一定量草酸钙固体,加热.加热过程中剩余固体的质量随时间变化如图所示.图中AB段发生反应的化学方程式为CaC2O4$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+CO↑,
DE段固体所含物质为CaO,或氧化钙(写化学式或物质名称均可,下同).
(2)实验二:探究草酸钙加热一段时间后剩余固体M的成分.
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| Ⅰ | 取少量固体M放入烧杯中,向烧杯中加足量 水,充分搅拌后静置 | 杯底有白色固体,且温度无明显变化(填“有”或“无” | 固体M中不含氧化钙 |
| Ⅱ | 再向烧杯中加足量稀盐酸并不断搅拌 | 有气泡体产生,固体全部溶解. | 固体M中一定含有的物质是碳酸钙,可能含有草酸钙CaCO3. |
质是碳酸钙和氧化钙.
 2016年3月30日参考消息网报道;中国快递垃圾惊人,年耗胶带169.5亿米,包装箱99亿个.为了获得买家“包装严密”好评,北京一家母婴用品网店,每个月使用近2万米的胶带包装,(1)胶带常用BOPP膜塑料作为基材,成分为聚丙烯(其化学组成可表示为
2016年3月30日参考消息网报道;中国快递垃圾惊人,年耗胶带169.5亿米,包装箱99亿个.为了获得买家“包装严密”好评,北京一家母婴用品网店,每个月使用近2万米的胶带包装,(1)胶带常用BOPP膜塑料作为基材,成分为聚丙烯(其化学组成可表示为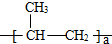 (a为正整数),BOPP膜塑料属于有机高分子(填“金属”、“有机高分子”、“硅酸盐”之一)材料.
(a为正整数),BOPP膜塑料属于有机高分子(填“金属”、“有机高分子”、“硅酸盐”之一)材料.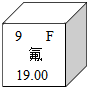 元素周期表中氟元素的有关信息如图所示,则氟的相对原子质量是19.00,氟原子的结构示意图为
元素周期表中氟元素的有关信息如图所示,则氟的相对原子质量是19.00,氟原子的结构示意图为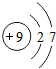 ,氟原子在化学反应中易得到(选填“得到”或”失去“)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为NaF.
,氟原子在化学反应中易得到(选填“得到”或”失去“)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为NaF.