题目内容
1.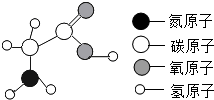 甘氨酸有独特的甜味,能缓和酸、碱味,掩盖食品中添加糖精的苦味并增强甜味.以甘氨酸为主要原料生产的含乳饮料,对青少年及儿童的正常生长发育很容易带来不利影响.甘氨酸分子结构模型如图所示,根据模型判断关于甘氨酸的叙述错误的是( )
甘氨酸有独特的甜味,能缓和酸、碱味,掩盖食品中添加糖精的苦味并增强甜味.以甘氨酸为主要原料生产的含乳饮料,对青少年及儿童的正常生长发育很容易带来不利影响.甘氨酸分子结构模型如图所示,根据模型判断关于甘氨酸的叙述错误的是( )| A. | 由碳、氢、氧、氮四种元素组成 | |
| B. | 氢元素的质量分数最大 | |
| C. | 甘氨酸化学式为C2H5O2N | |
| D. | 甘氨酸中碳元素与氧元素质量比为3:4 |
分析 A.根据化学式的意义来分析;
B.根据化合物中元素质量分数的大小比较方法来分析;
C.根据分子结构来分析;
D.根据化合物中元素质量比的计算方法来分析.
解答 解:由分子结构示意图可知,该物质的一个分子中含有2个碳原子、5个氢原子、2个氧原子、1个氮原子,其化学式为:C2H5O2N.
A.由化学式可知,甘氨酸是由碳、氢、氧、氮四种元素组成的,故正确;
B.甘氨酸中,碳、氢、氮、氧四种元素的质量比为:(12×2):(1×5):(16×2):14=24:5:32:14,可见其中氢元素的质量分数最小,故错误;
C.由分子结构示意图可知,该物质的一个分子中含有2个碳原子、5个氢原子、2个氧原子、1个氮原子,其化学式为:C2H5O2N,故正确;
D.根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;可得甘氨酸中碳、氧的质量比为:(12×2):(16×2)=3:4,故正确.
故选B.
点评 学会仔细读取物质的分子结构模型图,并根据模型能直观地看出构成物质的分子的构成,是解答此类题的关键.

练习册系列答案
相关题目
18.下列有关CO2和CO的知识归纳,正确的是( )
| A. | 组成:都是由碳和氧两种元素组成的 | |
| B. | 性质:都能使澄清石灰水变浑浊 | |
| C. | 用途:都可以用于冶炼金属 | |
| D. | 鉴别:可以用观察颜色的方法鉴别 |
9.为除去CO2中含有的少量CO杂质,下列操作中正确的是( )
| A. | 将气体通过灼热氧化铜 | B. | 将气体通入澄清石灰水中 | ||
| C. | 将气体通入硫酸溶液中 | D. | 将气体点燃 |
10.下列粒子结构示意图中表示阳离子的是( )
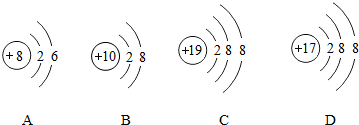

| A. | 它们表示的是同一种元素 | |
| B. | 它们的核外电子数相同 | |
| C. | 它们都具有相对稳定的结构 | |
| D. | 它们依次表示原子、原子、阳离子、阴离子 |
11.下列各组物质的鉴别方法错误的是( )
| A. | 用肥皂水鉴别硬水利软水 | |
| B. | 用闻气味的方法鉴别白酒和白醋 | |
| C. | 用水鉴别氢氧化钠同体和硝酸铵固体 | |
| D. | 用观察颜色的方法鉴别黄铜(铜锌合金)和黄金 |