题目内容
11.分析推理是化学中常用的思维方法,下列分析推理中正确的是( )| A. | 碳酸氢钠溶于水后显碱性,所以它是一种碱 | |
| B. | 白醋的pH值小于7,所以它呈酸性 | |
| C. | 某物质在20℃时溶解度是30g,所以在20℃时,溶质为30g的该物质的溶液一定是饱和溶液 | |
| D. | 氧化物是指氧元素与另一种化学元素组成的化合物,所以含有氧元素的化合物都是氧化物 |
分析 A、根据碱、盐的概念进行分析.
B、根据溶液的pH和酸碱性的关系进行分析判断.
C、根据溶解度的概念进行分析判断.
D、根据氧化物的概念进行分析判断.
解答 解:A、碳酸氢钠属于盐,故选项推理错误.
B、白醋的pH值小于7,所以它呈酸性,故选项推理正确.
C、某物质在20℃时溶解度是30g,说明在20℃时,30g该物质溶解在100g水中形成饱和溶液,若溶解在大于100g的水里则是不饱和溶液,故选项推理错误.
D、氧化物是指氧元素与另一种化学元素组成的化合物,但含有氧元素的化合物不都是氧化物,例如氯酸钾,故选项推理错误.
故选:B.
点评 本题难度不大,掌握物质分类的知识、溶解度的概念以及溶液的酸碱性和pH 的关系等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列图示中,化学实验基本操作正确的是( )
| A. |  向氢氧化钠溶液中滴加酚酞 | B. |  溶解氯化钠 | ||
| C. |  铁丝在O2中燃烧 | D. |  CO2的检验 |
6.潜水逐渐发展成为一项以在水下活动为主要内容,从而达到锻炼身体、休闲娱乐的目的休闲运动,广为大众所喜爱.潜水人员一般都会身穿潜水服、背着氧气罐下水,下列有关说法正确的是( )
| A. | 氧气罐中的氧气可以供给人呼吸 | B. | 水中氧气的含量为0 | ||
| C. | 氧气被压缩后分子的体积变小了 | D. | 氧气只能以气体的形式存在 |
16.下列措施中,有利于水生态环境的是( )
| A. | 大力推广使用含磷洗衣粉 | B. | 用未经处理的污水灌溉农田 | ||
| C. | 向河水中倾倒84消毒液杀毒 | D. | 合理使用农药 |
3.金属X与Ag2SO4反应的化学方程式为:X+Ag2SO4═XSO4+2Ag.下列说法中正确的是…( )
| A. | 金属X可能是钾 | |
| B. | Ag的化学性质比金属X活泼 | |
| C. | 金属X在金属活动性顺序里面一定排在氢后面 | |
| D. | 反应前后,Ag的化合价发生了改变 |
1.在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表:
(1)m=8;
(2)该反应的基本反应类型为化合反应.
| 物 质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 反应后的质量(g) | 12 | 1 | m | 14 |
(2)该反应的基本反应类型为化合反应.
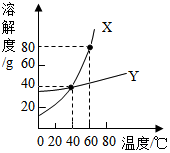 X、Y两种固体物质的溶解度曲线如图所示,回答下列问题:
X、Y两种固体物质的溶解度曲线如图所示,回答下列问题: