题目内容
11.研究性学习在实验室进行了化学实验,向一盛有镁和铜混合物的烧杯中加入一定量的稀盐酸,充分反应后,观察到烧杯中有固体剩余,对反应后所得溶液中溶质的成分进行探究.(1)写出上述烧杯中发生反应的化学方程式2HCl+Mg═MgCl2+H2↑.
(2)对反应后所得溶液中溶质的成分进行猜想,请你再补充一种猜想.
【猜想】小光猜想:溶质为氯化镁;
小红猜想:溶质为氯化铜和氯化镁;
你的猜想:溶质为氯化镁和氯化氢.
(3)【讨论】你认为小红的猜想不合理,理由是由于活动性由于铜在H后面,所以铜不能与盐酸反应,所以溶质中不可能有氯化铜.
(4)【实验】若你的猜想正确,设计一种实验方案证明你的猜想并完成下表:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后溶液:滴加几滴石蕊试液 | 溶液变红色 | 你的猜想正确 |
分析 (1)镁与盐酸反应生成氯化镁和氢气;
(2)根据镁与盐酸反应情况分析;
(3)根据金属的活动性分析;
(4)根据氢离子的验证方法分析;
(5)显酸性的溶液能够腐蚀下水道.
解答 解:(1)镁与盐酸反应生成氯化镁和氢气,化学方程式为2HCl+Mg═MgCl2+H2↑;
(2)镁与盐酸反应可能恰好反应也可能其中一种过量,如果盐酸过量时,溶质为氯化镁和氯化氢;
(3)由于活动性铜在H后面,所以铜不能与盐酸反应,所以溶质中不可能有氯化铜;
(4)要验证有盐酸的存在,使用紫色石蕊试液可以检验废液中是否含有呈酸性的盐酸;根据盐酸的性质,也可以选择活泼金属单质或碳酸盐检验废液中是否含有盐酸;
(5)通过以上探究,如果该废液未经处理直接倒入下水道,可能造成的危害是腐蚀下水道.
故答案为(1)2HCl+Mg═MgCl2+H2↑;
(2)氯化镁和氯化氢;
(3)小红;由于活动性由于铜在H后面,所以铜不能与盐酸反应,所以溶质中不可能有氯化铜;
(4)
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后溶液:滴加几滴石蕊试液 | 溶液变红色 | 你的猜想正确 |
点评 本题主要考查酸的性质,其中盐酸的性质有:可以使酸碱指示剂石蕊变红,可与活泼金属置换出氢气,可与金属氧化物发生复分解反应,可与碱发生中和反应,可与碳酸盐反应放出二氧化碳.

练习册系列答案
相关题目
19.下列说法正确的是( )
| A. | 空气的成分按体积计算氮气最多 | |
| B. | 催化剂只能加快化学反应速率 | |
| C. | 植物叶片发黄应施加磷肥 | |
| D. | 碳酸氢钠俗称苏打,是发酵粉成分之一 |
5.下列实验操作正确的是( )
| A. | 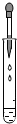 滴加液体 | B. | 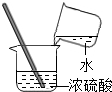 稀释浓硫酸 | ||
| C. | 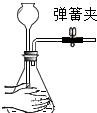 检查气密性 | D. | 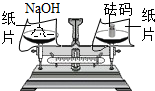 称量NaOH固体 |
12.规范的实验操作是进行科学探究的重要保障,下列实验操作不规范科学的是( )
| A. | 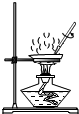 蒸发结晶 | B. | 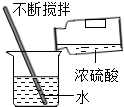 稀释浓硫酸 | C. | 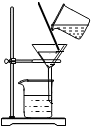 过滤 | D. | 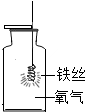 铁丝在氧气中燃 |
9.粗盐提纯实验中,下图操作错误的是( )
| A. |  称量 | B. | 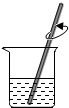 溶解 | C. | 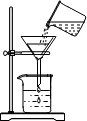 过滤 | D. | 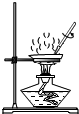 蒸发 |
 如图为某制药厂生产的高钙片标签上的部分文字,请阅读后回答:
如图为某制药厂生产的高钙片标签上的部分文字,请阅读后回答: