题目内容
18.工业上用10t含一定杂质的石灰石(主要成分是碳酸钙)高温燃烧制生石灰,若得到生石灰的质量为4.48t,则石灰石中碳酸钙的质量分数为( )| A. | 80% | B. | 70% | C. | 44.8% | D. | 56% |
分析 碳酸钙高温下分解生成氧化钙(生石灰)和二氧化碳,由生成生石灰的质量,由反应的化学方程式计算出参加反应的碳酸钙的质量即可.
解答 解:设参加反应的碳酸钙的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
x 4.48t
$\frac{100}{56}=\frac{x}{4.48t}$ x=8t
石灰石中碳酸钙的质量分数为$\frac{8t}{10t}×$100%=80%.
故选:A.
点评 本题难度不大,掌握利用化学方程式的简单计算并能灵活运用是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8. 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用.
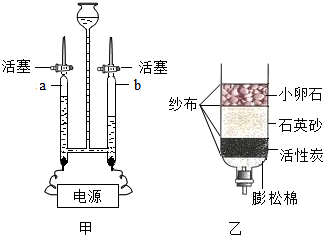
(1)电解水的实验掲示了水的组成.其反应的符号表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;甲图中检验a玻璃管内产生气体的方法是将带火星的木条伸入试管中,复燃则证明是氧气.
(2)某同学自制如图乙所示简易净水器,图中活性炭的主要作用是吸附.
(3)衣服上沾有的油污可用汽油洗去,是因为汽油能溶解(填“溶解”或“乳化”)油污.
(4)根据如表回答问题:
①20℃时,向两个分别盛有35g硝酸钾和氯化铵的烧杯中,各加入lOOg水,充分溶解后,为饱和溶液的是硝酸钾溶液;
②只用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液.下列说法正确的是BD.
A.溶液中溶质的质量不变 B.溶液中溶质的质量分数可能增大
C.溶液的质量可能不变 D.可升高温度或增加溶剂.
 水和溶液在生命活动和生产、生活中起着十分重要的作用.
水和溶液在生命活动和生产、生活中起着十分重要的作用.(1)电解水的实验掲示了水的组成.其反应的符号表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;甲图中检验a玻璃管内产生气体的方法是将带火星的木条伸入试管中,复燃则证明是氧气.
(2)某同学自制如图乙所示简易净水器,图中活性炭的主要作用是吸附.
(3)衣服上沾有的油污可用汽油洗去,是因为汽油能溶解(填“溶解”或“乳化”)油污.
(4)根据如表回答问题:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 100g水中最多 可溶解/g | 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| 氯化铵 | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
②只用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液.下列说法正确的是BD.
A.溶液中溶质的质量不变 B.溶液中溶质的质量分数可能增大
C.溶液的质量可能不变 D.可升高温度或增加溶剂.
9.下列变化中属于是物理变化的是( )
| A. | 水蒸发 | B. | 电解水 | C. | 红磷燃烧 | D. | 苹果腐烂 |
6.下列关于空气的说法中,正确的是( )
| A. | 按质量计算.空气中含有氮气$\frac{4}{5}$.含有氧气$\frac{1}{5}$ | |
| B. | 空气中的稀有气体常用作灭火剂 | |
| C. | 空气是人类宝贵的自然资源 | |
| D. | 空气被压缩时体积变小是化学变化 |
3.在密闭的容器中燃烧某物质,生成了二氧化碳和水,这一实验说明了( )
| A. | 该物质必定是由碳、氢、氧三种元素组成的 | |
| B. | 该物质分子是由碳原子和水分子构成的 | |
| C. | 该物质是炭黑和水组成的混合物 | |
| D. | 该物质可能是由碳元素和氢元素组成的纯净物 |
7.要除去下列物质中含有的少量杂质,所选用的方法正确的是( )
| 选项 | 物质 | 杂质 | 所用方法 |
| A | Fe3O4 | C | 高温加热 |
| B | 高锰酸钾 | 二氧化锰 | 加热 |
| C | 碳酸钙 | 氯化钙 | 溶解,过滤,洗涤,干燥 |
| D | 氮气 | 氧气 | 通过灼烧的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
14.化学是一门以实验为基础的科学,实验必须按照一定规则进行.下列实验的操作先后顺序不正确的是( )
| A. | 点燃可燃性气体前,应先检验气体的纯度,后点燃 | |
| B. | 实验室用高锰酸钾制取氧气实验结束时,应先将导管移出水面,后熄灭酒精灯 | |
| C. | 实验室制取O2、H2、CO2等气体时,应先先往装置中装入药品,后检查装置的气密性 | |
| D. | 做铁丝在氧气瓶中的燃烧实验时,应先在瓶底放些水或铺一层沙,再引燃铁丝 |