题目内容
根据四氧化三铁Fe3O4的化学式进行计算.
(1)四氧化三铁的相对分子质量
(2)四氧化三铁中铁、氧两种元素的质量比
(3)四氧化三铁中铁的质量分数
(4)232吨四氧化三铁中含铁多少吨.
(1)四氧化三铁的相对分子质量
(2)四氧化三铁中铁、氧两种元素的质量比
(3)四氧化三铁中铁的质量分数
(4)232吨四氧化三铁中含铁多少吨.
考点:相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)相对分子质量=相对原子质量与相应原子个数的乘积和;
(2)元素质量比=相对原子质量与相应原子个数的乘积比;
(3)某元素质量分数=
×100%;
(4)纯净物中元素的质量=纯净物的质量×元素的质量分数.
(2)元素质量比=相对原子质量与相应原子个数的乘积比;
(3)某元素质量分数=
| 该原子的相对原子质量×该原子个数 |
| 该物质的相对分子质量 |
(4)纯净物中元素的质量=纯净物的质量×元素的质量分数.
解答:解:(1)相对分子质量=相对原子质量与相应原子个数的乘积和,则四氧化三铁的相对分子质量=56×3+16×4=232;
(2)元素质量比=相对原子质量与相应原子个数的乘积比,所以四氧化三铁中铁、氧两种元素的质量比=(56×3):(16×4)=168:64=21:8;
(3)某元素质量分数=
×100%,所以四氧化三铁中铁的质量分数=
×100%≈72.4%;
(4)纯净物中元素的质量=纯净物的质量×元素的质量分数,则232吨四氧化三铁中含铁的质量是232g×
×100%=168g;
故答案为:(1)四氧化三铁的相对分子质量是232;
(2)四氧化三铁中铁、氧两种元素的质量比是21:8;
(3)四氧化三铁中铁的质量分数是72.4%;
(4)232吨四氧化三铁中含铁168g.
(2)元素质量比=相对原子质量与相应原子个数的乘积比,所以四氧化三铁中铁、氧两种元素的质量比=(56×3):(16×4)=168:64=21:8;
(3)某元素质量分数=
| 该原子的相对原子质量×该原子个数 |
| 该物质的相对分子质量 |
| 56×3 |
| 232 |
(4)纯净物中元素的质量=纯净物的质量×元素的质量分数,则232吨四氧化三铁中含铁的质量是232g×
| 56×3 |
| 232 |
故答案为:(1)四氧化三铁的相对分子质量是232;
(2)四氧化三铁中铁、氧两种元素的质量比是21:8;
(3)四氧化三铁中铁的质量分数是72.4%;
(4)232吨四氧化三铁中含铁168g.
点评:明确依据物质的化学式的相关计算方法,并能结合化学式正确分析解答.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目


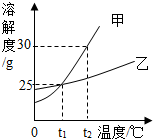 甲、乙两物质的溶解度曲线如图所示,请据图回答下列问题.
甲、乙两物质的溶解度曲线如图所示,请据图回答下列问题.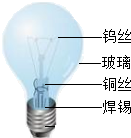 没有金属,生活是难以想象的.请你根据对金属和金属材料的认识,回答下列问题:
没有金属,生活是难以想象的.请你根据对金属和金属材料的认识,回答下列问题: