题目内容
9.稀盐酸与稀硫酸具有许多相似化学性质的原因是溶液中含有相同的H+,将锈铁钉放入稀硫酸中,使铁锈消失的化学方程式Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;过一会儿有气泡冒出,该反应的化学方程式Fe+H2SO4=FeSO4+H2↑.分析 根据酸是电离时产生的阳离子全部是氢离子的化合物,铁锈的主要成分是氧化铁,把生锈的铁钉放到足量的稀硫酸中,表面的铁锈先与硫酸反应,当铁锈完全反应完后,铁继续与硫酸酸反应,据此写出反应的化学方程式即可.
解答 解:酸是电离时产生的阳离子全部是氢离子的化合物,稀盐酸与稀硫酸具有许多相似化学性质的原因是溶液中含有相同的H+.
铁锈的主要成分是氧化铁,将锈铁钉放入稀硫酸中,铁锈的主要成分氧化铁与稀硫酸反应生成硫酸铁和水,会观察到铁锈逐渐溶解,溶液变黄;反应的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;当铁锈完全反应后,铁与稀硫酸发生反应生成硫酸亚铁与氢气,观察到的现象是铁钉表面有气泡产生;反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑.
故答案为:溶液中含有相同的H+;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;Fe+H2SO4=FeSO4+H2↑.
点评 本题难度不大,主要考查酸的化学性质,掌握铁锈的主要成分、酸的化学性质、化学方程式的书写等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列应用的原理(用化学方程式表示)及基本反应类型均正确的是( )
| A. | 用赤铁矿高炉炼铁 Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 置换反应 | |
| B. | 向硝酸铵中加入熟石灰研磨 NH4NO3+Ca(OH)2═Ca(NO3)2+NH3↑+H2O 复分解反应 | |
| C. | 闻气味鉴别碳铵 NH4HCO3═NH3↑+H2O+CO2↑ 分解反应 | |
| D. | 点燃酒精灯 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 |
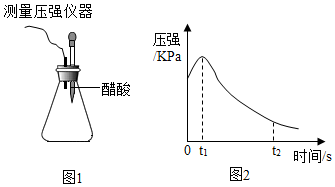
4.某研究小组为探究铁制品中的杂质含量和接触液体的酸性强弱对铁发生腐蚀的影响,将混合均匀的新制铁粉和碳粉(代替杂质)置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
(1)日常使用的铁制品都是铁的合金.铁合金中生铁的含碳量为2%~4.3%.
(2)请完成以下实验设计表(填写表中空白格):
(3)编号①实验测得容器中压强随时间变化如图2.t2时,容器中压强明显小于起始压强,其原因是随着时间的进行,铁粉生锈消耗了装置内的氧气,导致压强降低.
(4)该小组认为图2中0~t1时压强变大的原因有以下可能:
①铁与醋酸发生反应产生了氢气气体(填名称).
②铁与醋酸反应放热.

(1)日常使用的铁制品都是铁的合金.铁合金中生铁的含碳量为2%~4.3%.
(2)请完成以下实验设计表(填写表中空白格):
| 编号 | 实验目的 | 铁粉/g | 碳粉/g | 醋酸浓度/% |
| ① | 为以下实验作参照 | 2.0 | 0.5 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 20.0 | |
| ③ | 2.0 | 0.2 | 90.0 |
(4)该小组认为图2中0~t1时压强变大的原因有以下可能:
①铁与醋酸发生反应产生了氢气气体(填名称).
②铁与醋酸反应放热.
14.下列物质的用途利用了物质的化学性质的是( )
| A. | 活性炭净水 | B. | 金刚石做钻头 | ||
| C. | 石墨制铅笔 | D. | 熟石灰改良酸性土壤 |
18.下列属于纯净物的是( )
| A. | 洁净的空气 | B. | 氯化钠溶液 | C. | 冰水混合物 | D. | 黄铜 |


