题目内容
17.如图所示的三个实验可验证酸与碱能发生反应.
(1)实验一通过观察到氢氧化铁与稀盐酸反应的现象,验证了酸与碱能发生反应.
(2)实验二通过两只试管中的现象对比,可以判断稀盐酸与Ca(OH)2能发生反应,该实验除需控制所加水和稀盐酸的温度,体积相同外,还需控制氢氧化钙粉末的质量相同.
(3)实验三中,加入X可验证稀硫酸与碱能发生反应,符合此条件的X是下列物质中的A.
A、酚酞 B、铜丝 C、Ba(NO3)2.
分析 (1)据氢氧化钠与氯化铁反应生成氢氧化铁红褐色沉淀分析,据实验现象推测结论;
(2)据控制变量法分析;
(3)据碱与酸的化学性质回答.
解答 解:(1)氢氧化钠与氯化铁反应生成氢氧化铁红褐色沉淀,根据加入稀盐酸以后的红褐色沉淀逐渐消失,溶液变为黄色,推测酸与碱发生了化学反应;
(2)由控制变量法分析,本实验中除了水和稀盐酸的种类不同外,其它各量必须保持相同,水和稀盐酸的温度、体积相同,还需控制氢氧化钙粉末的质量相同.
(3)A、在碱中加入过量的酸后,溶液显酸性,再加入酚酞后溶液仍为无色,说明碱已经不存在了,进而证明了酸与碱确实发生了反应,故符合;
B、无论氢氧化钠与硫酸反应与否,加入铜后都没有明显现象,故不符合;
C、由于硫酸是过量的,不管H2SO4和NaOH有没有发生反应,都会有白色沉淀产生,故不符合;
故选A.
故答案为:(1)氢氧化铁与稀盐酸反应;(2)氢氧化钙粉末的质量;(3)A.
点评 本题考查了酸碱的反应,有一定的难度,把握题中信息,做好分析即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列图象能正确反映实验过程中相应量变化的是( )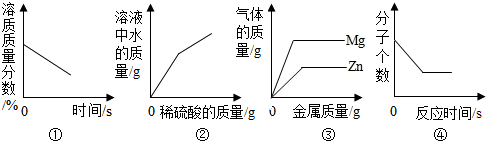
①将接近饱和的硝酸钾溶液缓慢降温
②向一定量的氢氧化钡溶液中加过量稀硫酸
③向等质量、等质量分数的稀盐酸中分别逐渐加入锌粉、镁粉至过量
④在密闭容器中点燃H2和O2的混合气体.

①将接近饱和的硝酸钾溶液缓慢降温
②向一定量的氢氧化钡溶液中加过量稀硫酸
③向等质量、等质量分数的稀盐酸中分别逐渐加入锌粉、镁粉至过量
④在密闭容器中点燃H2和O2的混合气体.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
12.不含氢、氧、碳三种元素的化合物,可能属于( )
| A. | 酸 | B. | 碱 | C. | 有机物 | D. | 盐 |
2. 某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
 某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )
某校化学小组在利用盐酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示,下列说法正确的是( )| A. | 图中a点所示溶液呈酸性 | |
| B. | 图中c点所示溶液中阳离子只有H+ | |
| C. | 图中a点所示溶液中,含有的溶质是NaCl和NaOH | |
| D. | 该实验是将氢氧化钠溶液逐滴滴入到盛有盐酸的烧杯中 |
9.为除去下列物质中的杂质(括号内是杂质),下列操作方法不正确的是( )
| 选项 | 物质 | 操作方法 |
| A | Cu(Fe) | 加入过量稀盐酸,充分反应后过滤 |
| B | NaOH溶液[Ca(OH)2溶液] | 加适量的碳酸钠溶液,充分搅拌后过滤 |
| C | NaCl溶液(Na2SO4溶液) | 加入适量的氯化钡溶液,充分反应后过滤 |
| D | CO2(HCl) | 通入足量的氢氧化钠溶液,干燥 |
| A. | A | B. | B | C. | C | D. | D |
6.下列描述与实验事实相符的是( )
| A. | 硝酸铵溶于水,溶液温度升高 | |
| B. | 红磷在空气中燃烧产生大量的烟雾 | |
| C. | 将铁锈放入稀硫酸中,铁锈逐渐消失,溶液变为黄色 | |
| D. | 氢气在空气中燃烧,发出明亮的蓝紫色的光 |


 小明同学取14%的硫酸溶液70g于烧杯中,然后向烧杯中慢慢加入10g氧化铜粉末并不断搅拌,测得烧杯中溶液的质量与加入氧化铜粉末的质量关系如图所示.求:
小明同学取14%的硫酸溶液70g于烧杯中,然后向烧杯中慢慢加入10g氧化铜粉末并不断搅拌,测得烧杯中溶液的质量与加入氧化铜粉末的质量关系如图所示.求: