题目内容
(2012?金山区一模)王老师要用含杂质质量分数为20%的大理石与足量的稀盐酸反应,制备10瓶二氧化碳气体.已知:
①集气瓶的体积为100mL;
②大理石中杂质不与稀盐酸反应;
③常温常压下二氧化碳的密度为1.98g/L.
计算李王师需要准备大理石的最少质量.
①集气瓶的体积为100mL;
②大理石中杂质不与稀盐酸反应;
③常温常压下二氧化碳的密度为1.98g/L.
计算李王师需要准备大理石的最少质量.
分析:根据二氧化碳的体积和密度算出质量,再根据方程式计算出碳酸钙的质量,再除以大理石中碳酸钙的质量分数即可.
解答:解:反应生成的CO2质量=10×100 mL×10-3L/mL×1.98 g/L=1.98 g
设:CaCO3质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 1.98 g
=
x=4.5g
需要准备大理石质量=
=5.625g
答:需要准备大理石的最少质量为5.625g.
设:CaCO3质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 1.98 g
| 100 |
| x |
| 44 |
| 1.98g |
x=4.5g
需要准备大理石质量=
| 4.5g |
| 1-20% |
答:需要准备大理石的最少质量为5.625g.
点评:解答本题的关键是要根据二氧化碳的体积和密度计算出质量,要注意体积、密度、质量的关系,还需要注意含杂质的质量.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
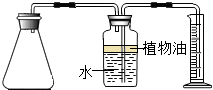 (2012?金山区一模)小明买了一种“汽泡爽”的冲调饮料.小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响.
(2012?金山区一模)小明买了一种“汽泡爽”的冲调饮料.小明观察了饮料说明后,他借助化学实验的方法,探究“汽泡爽”产生气体的成分,以及加水温度对产生气体量的影响.