题目内容
某化学活动小组与用溶质质量分数为98%的浓硫酸,配置某实验所需的溶质质量分数为19.6%的稀硫酸,并确定所配置的稀硫酸是否符合实验要求:
(1)配置稀硫酸:
①计算配置200g的稀硫酸需浓硫酸 g;
②正确的配置方法是 ;
(2)测定所配制稀硫酸的溶质质量分数:取50g所配置的稀硫酸于烧杯中,滴入几滴酚酞试液后,逐滴滴入溶质质量分数为10%的NaOH溶液,当消耗77.6gNaOH溶液时恰好完全反应,
①实验中观察到 ,说明恰好完全反应;
②计算所配置稀硫酸的溶质的质量分数(请写出计算步骤,得数精确到0.1%).
(1)配置稀硫酸:
①计算配置200g的稀硫酸需浓硫酸
②正确的配置方法是
(2)测定所配制稀硫酸的溶质质量分数:取50g所配置的稀硫酸于烧杯中,滴入几滴酚酞试液后,逐滴滴入溶质质量分数为10%的NaOH溶液,当消耗77.6gNaOH溶液时恰好完全反应,
①实验中观察到
②计算所配置稀硫酸的溶质的质量分数(请写出计算步骤,得数精确到0.1%).
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据溶质质量不变求出配制200g的稀硫酸需浓硫酸的质量,根据稀释浓硫酸的方法,分析配制的方法.
(2)根据酸与碱恰好反应时所需的氢氧化钠的质量求出50g硫酸中溶质的质质量,最后求出稀硫酸的溶质的质量分数.
(2)根据酸与碱恰好反应时所需的氢氧化钠的质量求出50g硫酸中溶质的质质量,最后求出稀硫酸的溶质的质量分数.
解答:解:(1)①设配制200g的稀硫酸需浓硫酸的质量为X.
200g×19.6%=X×98% 解得:X=40g,需要水的质量为:200g-40g=160g,则需水的体积是160mL.
②正确的配置方法是:用量筒量量取160mL的水倒入烧杯中,再称量40g室温浓硫酸沿器壁慢慢注入水中,并不断搅拌.
(2)①根据酚酞的变色可知,实验中观察到溶液颜色刚刚变为红色,说明恰好完全反应;
②所消耗的氢氧化钠溶液中溶质的质量为:76.6g×10%=7.66g
设所配置稀硫酸的溶质的质量为y
2NaOH+H2SO4 ═Na2SO4 +2H2O
80 98
76、6g y
=
解得:y=9.3835g
所配置稀硫酸的溶质的质量分数为:
×100%≈18.8%.
故答为:(1)①40;②用量筒量取160mL到在烧杯中,再称量40g室温浓硫酸沿器壁慢慢注入水中,并不断搅拌;(2)①溶液颜色刚刚变为红色;②所配置稀硫酸的溶质的质量分数为18.85%.
200g×19.6%=X×98% 解得:X=40g,需要水的质量为:200g-40g=160g,则需水的体积是160mL.
②正确的配置方法是:用量筒量量取160mL的水倒入烧杯中,再称量40g室温浓硫酸沿器壁慢慢注入水中,并不断搅拌.
(2)①根据酚酞的变色可知,实验中观察到溶液颜色刚刚变为红色,说明恰好完全反应;
②所消耗的氢氧化钠溶液中溶质的质量为:76.6g×10%=7.66g
设所配置稀硫酸的溶质的质量为y
2NaOH+H2SO4 ═Na2SO4 +2H2O
80 98
76、6g y
| 80 |
| 98 |
| 76.6g |
| y |
所配置稀硫酸的溶质的质量分数为:
| 9.3835g |
| 50g |
故答为:(1)①40;②用量筒量取160mL到在烧杯中,再称量40g室温浓硫酸沿器壁慢慢注入水中,并不断搅拌;(2)①溶液颜色刚刚变为红色;②所配置稀硫酸的溶质的质量分数为18.85%.
点评:酸碱中和可改变溶液的酸碱度,向酸溶液中滴加碱溶液时,溶液的酸碱度逐渐变大至等于7,滴加过量则大于7;向碱溶液中滴加酸时,溶液酸碱度逐渐减小至等于7,酸过量溶液pH值小于7.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
某气体完全燃烧,产物中含有二氧化碳和水,则该气体组成中( )
| A、可能含有碳、氧元素 |
| B、一定含有氧元素 |
| C、一定含有碳、氢二种元素 |
| D、可能含有碳、氢、氧元素 |
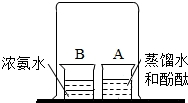 如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞溶液,在小烧杯B中装入30mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起.过一段时间烧杯A中溶液变红色,该实验说明分子具有的性质是
如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞溶液,在小烧杯B中装入30mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起.过一段时间烧杯A中溶液变红色,该实验说明分子具有的性质是