题目内容
有铜、锌、氧化锌的混合物共18克,向混合物中加入100克14.6%的稀盐酸后,恰好使各反应物反应完全,同时收集到气体0.2克.试求混合物中铜、锌、氧化锌的质量各为多少克?
【答案】分析:因为三种物质中只有锌能够与盐酸反应生成氢气,所以利用所得的气体质量可求出锌的质量,利用盐酸可以和锌、氧化锌反应,结合与之反应的氯化氢的质量可以求出氧化锌的质量,据此分析解答即可
解答:解:设锌的质量是x,与之反应的氯化氢质量是y
Zn+2HCl=ZnCl2+H2↑
65 73 2
x y 0.2g
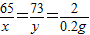
x=6.5g y=7.3g
所以与氧化锌反应的氯化氢的质量是100g×14.6%-7.3g=7.3g
设氧化锌的质量是z
ZnO+2HCl=ZnCl2+H2O↑
81 73
z 7.3g
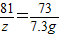
z=8.1g
固体中铜不与盐酸反应,其质量为18g-6.5g-8.1g=3.4g
答:混合物中铜、锌、氧化锌的质量各为:6.5克、8.1克、3.4克;
点评:此题难度不大,主要是利用化学方程式的有关计算以及判断反应的具体情况;
解答:解:设锌的质量是x,与之反应的氯化氢质量是y
Zn+2HCl=ZnCl2+H2↑
65 73 2
x y 0.2g
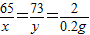
x=6.5g y=7.3g
所以与氧化锌反应的氯化氢的质量是100g×14.6%-7.3g=7.3g
设氧化锌的质量是z
ZnO+2HCl=ZnCl2+H2O↑
81 73
z 7.3g
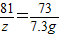
z=8.1g
固体中铜不与盐酸反应,其质量为18g-6.5g-8.1g=3.4g
答:混合物中铜、锌、氧化锌的质量各为:6.5克、8.1克、3.4克;
点评:此题难度不大,主要是利用化学方程式的有关计算以及判断反应的具体情况;

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
 26、小芳从废干电池中回收有关物质并进行探究,请你参与研究.
26、小芳从废干电池中回收有关物质并进行探究,请你参与研究. 小芳从废干电池中回收有关物质并进行探究,请你参与研究.
小芳从废干电池中回收有关物质并进行探究,请你参与研究.