题目内容
2.甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )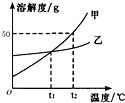
| A. | 要从甲的溶液中获得甲的晶体,可以采用降温结晶的方法 | |
| B. | 升高温度可以使甲的不饱和溶液变为饱和溶液 | |
| C. | t1℃时,甲、乙两种物质的饱和溶液中,溶质质量分数相等 | |
| D. | t1℃时,甲饱和溶液溶质质量分数为50% |
分析 根据已有的溶解度曲线的意义以及结晶的方法、溶质质量分数的计算进行分析解答即可.
解答 解:A、甲的溶解度随温度升高变化明显,故要从甲的溶液中获得甲的晶体,可以采用降温结晶的方法,正确;
B、升高温度甲的不饱和溶液仍然是不饱和溶液,错误;
C、t1℃时,甲和乙的溶解度相等,故甲、乙两种物质的饱和溶液中,溶质质量分数相等,正确;
D、t1℃时,甲的溶解度小于50g,故甲饱和溶液溶质质量分数不会为50%,错误;
故选AC.
点评 掌握溶解度曲线的意义是正确解答本题的关键.

练习册系列答案
相关题目
12.下列有关实验现象的叙述中,不正确的是( )
| A. | 镁条在空气中燃烧,发出耀眼的白光,生成白色固体 | |
| B. | 将二氧化碳通入紫色石蕊试液中,石蕊试液会变红 | |
| C. | 煤炉中煤层上方的火焰呈蓝色 | |
| D. | 木炭在氧气中燃烧生成黑色固体 |
17. 如图是甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
如图是甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
 如图是甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )
如图是甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )| A. | 10℃时,甲、乙两种物质的饱和溶液中溶质的质量相同 | |
| B. | 保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液 | |
| C. | 30℃时,将40g 甲物质加人50g水中,充分溶解后溶液的质量为80g | |
| D. | 10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大 |
7.下列只能表示微观意义的是( )
| A. | S | B. | SO2 | C. | 2CO2 | D. | H |
11.除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是( )
| A. | CuO(C)--在空气中灼烧 | |
| B. | CaCO3固体(CaO固体)--高温煅烧 | |
| C. | NaCl溶液(Na2CO3)--加入适量的澄清石灰水,过滤 | |
| D. | CO2气体(HCl气体)--依次通过足量的NaOH溶液和浓硫酸 |
12.有关物质性质的描述中,属于物理性质的是( )
| A. | 以粮食为原料能酿酒 | |
| B. | 二氧化碳能使澄清石灰水变浑浊 | |
| C. | 空气时没有颜色、没有其味道的气体 | |
| D. | 石灰石(或大理石)遇到盐酸后会生成二氧化碳和水 |
 归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).
归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应).