题目内容
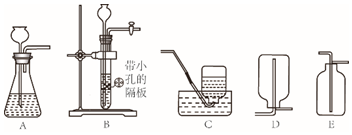
16.以下是在实验室里制取气体时常用的部分仪器.
(1)标号为e的仪器名称是酒精灯;
(2)在实验室里,用高锰酸钾来制取氧气,并用排水法收集,写出反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;制取装置中除选择的a、b、d、f、h、l、n外,还应选择如图所给仪器中的e、k、m.
(3)实验室用大理石与稀盐酸反应来制取二氧化碳气体,化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,要制取4.4g二氧化碳,需要10%的稀盐酸73g,实验后的液体中常常还有稀盐酸,加入过量的石灰石可得到只含CaCl2的溶液.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,该反应的反应物是固体,反应条件是加热,用排水法收集氧气进行分析;
(3)根据化学方程式和制取的二氧化碳质量进行计算.
根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,e是酒精灯;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应的反应物是固体,反应条件是加热,用排水法收集氧气,所以制取装置中除选择的a、b、d、f、h、l、n外,还应选择如图所给仪器中的e、k、m;
(3)设需要10%的稀盐酸为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
x×10% 4.4g
$\frac{73}{x×10%}$=$\frac{44}{4.4g}$
x=73g
碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,不用指示剂可以将盐酸完全反应,所以加入过量的石灰石可得到只含CaCl2的溶液.
故答案为:(1)酒精灯;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,e、k、m;
(3)73,石灰石.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
相关题目
16.失去标签的三瓶无色液体,分别是稀硫酸、蒸馏水、氢氧化钠溶液,一次性就能把它们区别开的试剂是( )
| A. | 无色酚酞试液 | B. | 硝酸钙溶液 | C. | 氯化钡溶液 | D. | 紫色石蕊试液 |
4.同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案.请你和他们一起完善下表的探究方案并回答有关问题.
(1)填写表格:
结论:金属活动性Al>Fe>Cu
(2)写出此实验中发生反应的两条化学方程式:Fe+2HCl═FeCl2+H2↑.2Al+3FeCl2=2AlCl3+3Fe.
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论.小华要补充的实验是把铜丝插入稀盐酸中.
(1)填写表格:
| 实验步骤 | 观察到的现象 |
| ①在试管中取少量盐酸,插入铁丝,充分作用. | 产生气泡,溶液变浅绿色 |
| ②在①所得的溶液中,插入铜丝,充分作用. | 无明显现象 |
| ③在②所得的溶液中插入铝丝,充分作用. | 铝丝表面会覆盖一层黑色物质,溶液变为无色 |
(2)写出此实验中发生反应的两条化学方程式:Fe+2HCl═FeCl2+H2↑.2Al+3FeCl2=2AlCl3+3Fe.
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论.小华要补充的实验是把铜丝插入稀盐酸中.
1.下列符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是( )
| A. | 2O | B. | H2 | C. | He | D. | Cl |
8.下列实验操作正确的是( )
| A. |  浓硫酸稀释 | B. |  向酒精灯里添加酒精 | ||
| C. |  称量氢氧化钠固体 | D. |  测定溶液的pH |