题目内容
下图分别与相应的操作过程相对应,其中正确的是
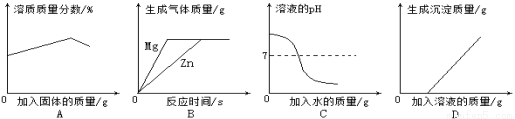
A.恒温下,向一接近饱和的硝酸钾溶液中不断加入硝酸钾晶体
B.向等质量、等溶质质量分数的稀硫酸中分别加入足量的镁片和锌片
C.向pH=10的氢氧化钙溶液中不断加水稀释
D.向含有硫酸的硫酸铜的混合溶液中加入过量的氢氧化钠溶液
B
【解析】
试题分析:A、温度不变,溶剂的量不变,饱和溶液无法继续溶解溶质,加入硝酸钾晶体溶质质量分数也不会改变,错误;B、等质量、等溶质质量分数的稀硫酸,即硫酸的量相同那么生成的氢气的量相同,Mg的活动性比Zn更强,那么Mg的反应速率更快,正确。C、向pH=10的氢氧化钙溶液中不断加水稀释,只是碱性会减弱pH值变小,但不会变成中性酸性,pH不会≤7,错误;D、含有硫酸的硫酸铜的混合溶液中硫酸铜的量是一定的,那么沉淀的质量不可能一直增加,错误。
考点:化学反应中量的变化

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案铀是原子弹重要原料,是核电站的重要燃料。下图是铀元素在元素周期表中铀元素的截图,下列有关说法错误的是

A.铀的元素符号为U B.铀属于非金属元素
C.铀原子的质子数为92 D.铀的相对原子质量为238.0
在研究酸和碱的化学性质时,某小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,试与他们一起完成实验方案的设计,实施和评价,并得出有关结论.
(1)探究稀硫酸与氢氧化钠溶液的反应:
当滴入几滴酚酞试液后,溶液由无色变为 色,根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为: .
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:
根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
上述设计的实验方案中,正确的是 (填“方案一”或“方案二”)
另外一个实验方案错误的原因是 ;
请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是 ,实验现象及结论是 .
如图所示,瓶中X为固体,把滴管内的液体Y滴入瓶中,插入水中的导管口一定没有气泡冒出的是

A | B | C | D | |
X | Zn | NaCl | CaO | NaOH |
Y | H2SO4 | H2O | H2O | H2O |



