题目内容
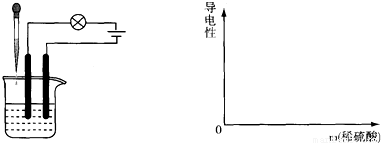
我们可以通过测定溶液的导电性来判断酸碱盐化合物水溶液的反应.如图所示:
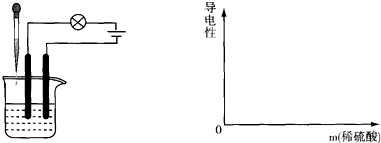
烧杯中盛放的是Ba(OH)2溶液,溶液中插入的为石墨电极,连接灯泡和电源.实验开始时灯泡是亮的,随着稀H2SO4的滴入,灯泡逐渐变暗,直至不亮.继续滴加稀H2SO4后,灯泡又能恢复变亮.实验中灯泡不亮的原因是,烧杯中没有自由移动________的缘故.溶液的导电性随H2SO4滴入的变化的曲线为(请作图)
写出该反应的化学方程式________.在该反应中,参加反应的“特殊的”离子为________(填离子符号).
离子 Ba(OH)2+H2SO4═BaSO4↓+2H2O Ba2+,SO42-,H+,OH-
分析:水溶液要想导电必须具有自由移动的带电的微粒,带电的微粒越多越容易导电,向稀硫酸中逐渐滴入氢氧化钡溶液,离子浓度逐渐减小,导电性逐渐降低,最后导电能力为零,所加物质过量就又能够导电了,溶液中溶液的导电性变化是强→弱(水有微弱的导电性)→强;根据氢氧化钡和硫酸反应生成硫酸钡和水进行解答.
解答:向稀硫酸溶液中慢慢滴加氢氧化钡溶液直至过量,由于发生了反应:Ba(OH)2+H2SO4═BaSO4↓+2H2O,随着氢氧化钡溶液的滴加,离子浓度逐渐减小,导电性逐渐降低,最后导电能力为零,也就是说恰好完全反应时没有自由移动的离子了,所加物质过量就又能够导电了,溶液中溶液的导电性变化是强→弱(水有微弱的导电性)→强,变化的曲线为: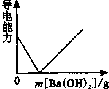 在该反应中,参加反应的“特殊的”离子为:Ba2+,SO42-,H+,OH-.
在该反应中,参加反应的“特殊的”离子为:Ba2+,SO42-,H+,OH-.
故答案为:离子;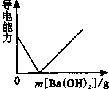 ;Ba(OH)2+H2SO4═BaSO4↓+2H2O;Ba2+,SO42-,H+,OH-.
;Ba(OH)2+H2SO4═BaSO4↓+2H2O;Ba2+,SO42-,H+,OH-.
点评:通过回答本题知道了两种物质反应后要想导电必须具有自由移动的离子,溶液的导电性强弱与离子浓度有关.
分析:水溶液要想导电必须具有自由移动的带电的微粒,带电的微粒越多越容易导电,向稀硫酸中逐渐滴入氢氧化钡溶液,离子浓度逐渐减小,导电性逐渐降低,最后导电能力为零,所加物质过量就又能够导电了,溶液中溶液的导电性变化是强→弱(水有微弱的导电性)→强;根据氢氧化钡和硫酸反应生成硫酸钡和水进行解答.
解答:向稀硫酸溶液中慢慢滴加氢氧化钡溶液直至过量,由于发生了反应:Ba(OH)2+H2SO4═BaSO4↓+2H2O,随着氢氧化钡溶液的滴加,离子浓度逐渐减小,导电性逐渐降低,最后导电能力为零,也就是说恰好完全反应时没有自由移动的离子了,所加物质过量就又能够导电了,溶液中溶液的导电性变化是强→弱(水有微弱的导电性)→强,变化的曲线为:
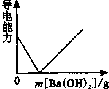 在该反应中,参加反应的“特殊的”离子为:Ba2+,SO42-,H+,OH-.
在该反应中,参加反应的“特殊的”离子为:Ba2+,SO42-,H+,OH-.故答案为:离子;
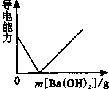 ;Ba(OH)2+H2SO4═BaSO4↓+2H2O;Ba2+,SO42-,H+,OH-.
;Ba(OH)2+H2SO4═BaSO4↓+2H2O;Ba2+,SO42-,H+,OH-.点评:通过回答本题知道了两种物质反应后要想导电必须具有自由移动的离子,溶液的导电性强弱与离子浓度有关.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
 化学是一门实验科学.我们可以通过观察肉眼可见的实验现象,再加上分析推理,来认识分子的性质和确认分子的真实存在.
化学是一门实验科学.我们可以通过观察肉眼可见的实验现象,再加上分析推理,来认识分子的性质和确认分子的真实存在.