题目内容
根据要求写出下列方程式,并注明基本反应类型.(1)铝制品抗腐蚀性强的原因______反应;
(2)高温时碳还原氧化铜______ 2Cu+CO2↑;置换
【答案】分析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;再根据反应特征确定反应类型.
解答:解:(1)铝能与空气中氧气反应在其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化,因此铝制品抗腐蚀性强,反应的化学方程式为4Al+3O2═2Al2O3;该反应符合“多变一”的特征,属于化合反应.
(2)高温时碳还原氧化铜生成铜和二氧化碳,反应的化学方程式为C+2CuO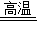 2Cu+CO2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
2Cu+CO2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
(3)过氧化钠(Na2O2)与二氧化碳反应生成一种碱性物质(碳酸钠)与氧气,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.
故答案为:(1)4Al+3O2═2Al2O3;化合;(2)C+2CuO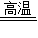 2Cu+CO2↑;置换;(3)2Na2O2+2CO2═2Na2CO3+O2.
2Cu+CO2↑;置换;(3)2Na2O2+2CO2═2Na2CO3+O2.
点评:本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法、四种基本反应类型的特征即可正确解答本题.
解答:解:(1)铝能与空气中氧气反应在其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化,因此铝制品抗腐蚀性强,反应的化学方程式为4Al+3O2═2Al2O3;该反应符合“多变一”的特征,属于化合反应.
(2)高温时碳还原氧化铜生成铜和二氧化碳,反应的化学方程式为C+2CuO
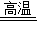 2Cu+CO2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
2Cu+CO2↑;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.(3)过氧化钠(Na2O2)与二氧化碳反应生成一种碱性物质(碳酸钠)与氧气,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.
故答案为:(1)4Al+3O2═2Al2O3;化合;(2)C+2CuO
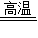 2Cu+CO2↑;置换;(3)2Na2O2+2CO2═2Na2CO3+O2.
2Cu+CO2↑;置换;(3)2Na2O2+2CO2═2Na2CO3+O2.点评:本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法、四种基本反应类型的特征即可正确解答本题.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目


