题目内容
下图是实验室常用的装置.请据图回答: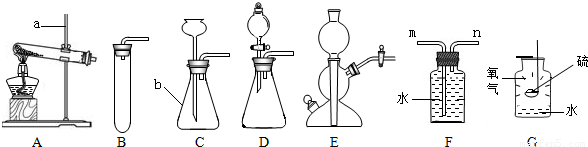
(1)写出仪器a的名称______、仪器b的名称______.
(2)写出用装置A制取氧气的化学方程式:______△2KCl+3O2↑,
【答案】分析:(1)根据常用仪器名称和用途解答;
(2)根据氯酸钾制取氧气的反应原理和反应类型的特点判断,并根据仪器特点判断所选仪器;
(3)根据硫在氧气中燃烧的现象及二氧化硫有毒和环保的角度回答;
(4)根据制取二氧化碳发生装置的特点选择,并根据装置特点分析其优越性;
(5)根据石灰石与稀盐酸的反应方程式及溶质的质量分数进行计算.
解答:解:(1)根据常用仪器名称和用途可知仪器分别为:铁架台,锥形瓶;
故答案为:铁架台,锥形瓶;
(2)氯酸钾在二氧化锰作催化剂,加热的条件下生成氯化钾和氧气,由一种物质生成两种物质,符合分解反应的特点,属于分解反应,氧气的密度比水小,所以,氧气应从n端通入,在m端接一个量筒测量排出水的体积即为生成氧气的体积;
故答案为:2KClO3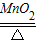 2KCl+3O2↑,分解反应,m;
2KCl+3O2↑,分解反应,m;
(3)物质燃烧的现象可从一光二热三生成进行回答,硫在氧气中燃烧发出明亮的蓝紫色火焰,产生刺激性气味的气体,放出热量,二氧化硫是一种大气污染物,溶于水生成亚硫酸,所以可在集气瓶内放一些水来吸收二氧化硫,防止污染空气;
故答案为:发出明亮的蓝紫色火焰,产生刺激性气味的气体,放出热量;吸收二氧化硫,防止生成二氧化硫外泄污染环境;
(4)实验室制取二氧化碳用石灰石与稀盐酸常温反应,属于“固液常温型”,所以可选择BCDE装置,E装置与B相比,可随时添加液体试剂(盐酸),并可使反应随时发生或停止,节约药品;
故答案为:BCDE;可随时添加液体试剂(盐酸),并可使反应随时发生或停止,节约药品;
(5)①CO2的物质的量=8.8克/44克/摩尔=0.2摩尔
设:需HCl为X摩尔
CaCO3+2HCl═CaCl2+CO2↑+H2O
2 1
X 0.2摩尔
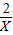 =
=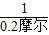
X=0.4(摩尔)
②该稀盐酸中HCl的质量分数为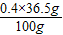 ×100%=14.6%.
×100%=14.6%.
点评:本题考查知识全面,既考查了装置的选取、反应原理、反应类型、物质燃烧的现象,又考查了根据方程式的计算,有一定难度,要细心分析.
(2)根据氯酸钾制取氧气的反应原理和反应类型的特点判断,并根据仪器特点判断所选仪器;
(3)根据硫在氧气中燃烧的现象及二氧化硫有毒和环保的角度回答;
(4)根据制取二氧化碳发生装置的特点选择,并根据装置特点分析其优越性;
(5)根据石灰石与稀盐酸的反应方程式及溶质的质量分数进行计算.
解答:解:(1)根据常用仪器名称和用途可知仪器分别为:铁架台,锥形瓶;
故答案为:铁架台,锥形瓶;
(2)氯酸钾在二氧化锰作催化剂,加热的条件下生成氯化钾和氧气,由一种物质生成两种物质,符合分解反应的特点,属于分解反应,氧气的密度比水小,所以,氧气应从n端通入,在m端接一个量筒测量排出水的体积即为生成氧气的体积;
故答案为:2KClO3
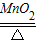 2KCl+3O2↑,分解反应,m;
2KCl+3O2↑,分解反应,m;(3)物质燃烧的现象可从一光二热三生成进行回答,硫在氧气中燃烧发出明亮的蓝紫色火焰,产生刺激性气味的气体,放出热量,二氧化硫是一种大气污染物,溶于水生成亚硫酸,所以可在集气瓶内放一些水来吸收二氧化硫,防止污染空气;
故答案为:发出明亮的蓝紫色火焰,产生刺激性气味的气体,放出热量;吸收二氧化硫,防止生成二氧化硫外泄污染环境;
(4)实验室制取二氧化碳用石灰石与稀盐酸常温反应,属于“固液常温型”,所以可选择BCDE装置,E装置与B相比,可随时添加液体试剂(盐酸),并可使反应随时发生或停止,节约药品;
故答案为:BCDE;可随时添加液体试剂(盐酸),并可使反应随时发生或停止,节约药品;
(5)①CO2的物质的量=8.8克/44克/摩尔=0.2摩尔
设:需HCl为X摩尔
CaCO3+2HCl═CaCl2+CO2↑+H2O
2 1
X 0.2摩尔
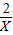 =
=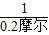
X=0.4(摩尔)
②该稀盐酸中HCl的质量分数为
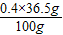 ×100%=14.6%.
×100%=14.6%.点评:本题考查知识全面,既考查了装置的选取、反应原理、反应类型、物质燃烧的现象,又考查了根据方程式的计算,有一定难度,要细心分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 K,然后用热毛巾捂住集气瓶,
K,然后用热毛巾捂住集气瓶,




 下图是实验室常用的装置。请据图回答:
下图是实验室常用的装置。请据图回答: