题目内容
把锌和铜的混合物50g和足量稀硫酸反应,可制得氢气1.1g,这种混合物里含锌________g和铜________g.
35.75 14.25
分析:根据金属的活动性顺序可知铜不能与稀硫酸产生氢气而锌能,据此可知生成的氢气即是锌反应产生的,所以依据化学方程式中氢气的质量可求出反应的锌的质量,进而可知铜的质量.
解答:设生成1.1g氢气时反应的锌的质量为x;
Zn+H2SO4=ZnSO4+H2↑
65 2
x 1.1g
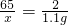
x=35.75g
铜的质量=50g-35.75g=14.25g
答:混合物中锌的质量为35.75g;铜的质量为14.25g.
故答案为:35.75;14.25.
点评:解答本题的关键是要知道铜与硫酸不反应,因为铜排在了氢的后面,只有排在氢前面的金属才能与酸反应产生氢气,据此依据化学方程式进行相关计算即可.
分析:根据金属的活动性顺序可知铜不能与稀硫酸产生氢气而锌能,据此可知生成的氢气即是锌反应产生的,所以依据化学方程式中氢气的质量可求出反应的锌的质量,进而可知铜的质量.
解答:设生成1.1g氢气时反应的锌的质量为x;
Zn+H2SO4=ZnSO4+H2↑
65 2
x 1.1g
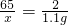
x=35.75g
铜的质量=50g-35.75g=14.25g
答:混合物中锌的质量为35.75g;铜的质量为14.25g.
故答案为:35.75;14.25.
点评:解答本题的关键是要知道铜与硫酸不反应,因为铜排在了氢的后面,只有排在氢前面的金属才能与酸反应产生氢气,据此依据化学方程式进行相关计算即可.

练习册系列答案
相关题目
