题目内容
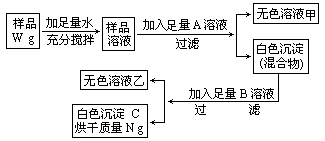
某氯化钠固体样品中含有少量碳酸钠杂质,为测定其中氯化钠的质量分数,可进行如图所示实验: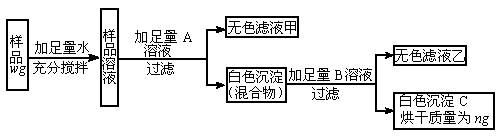
实验过程中用到的A溶液和B溶液可从下列溶液中选择:稀盐酸、稀硝酸、硝酸银溶液、烧碱溶液。
(1)推断加入的A溶液是________,加入的B溶液是________。
(2)固体样品中氯化钠的质量分数是________。
答案:
解析:
提示:
解析:
| 解答此题必须明确:为了测定氯化钠的质量分数,需将杂质与氯化钠分开。氯化钠可以选用硝酸银作试剂将它全部沉淀,但由于碳酸钠也与硝酸银产生碳酸银沉淀而发生干扰,因此需加稀硝酸排除干扰,所以加入的A溶液为硝酸银溶液,加入的B溶液为稀硝酸。氯化银不溶于稀硝酸,而碳酸银溶于稀硝酸,这样可以得到纯净的白色沉淀C(氯化银)ng,再根据化学方程式求氯化银的质量,进而求出氯化银的质量分数。
设样品中氯化钠的质量为x。 NaCl+AgNO3 58.5 143.5 x ng 58.5∶143.5=x∶ng,x= 样品中氯化钠的质量分数为: 答案:(1)AgNO3溶液 稀HNO3 (2)
|
提示:

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
为了将混有硫酸钠、碳酸氢铵(不稳定,受热易分解生成氨气、二氧化碳和水)的氯化钠提纯,某同学设计的实验流程如下:
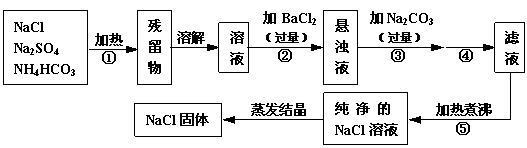 |
试回答下列问题:
(1)操作①的目的是 。操作②能否用硝酸钡溶液? (填“能”或“否”)。
(2)进行操作②后,如何判断SO 已除尽,方法是 。
已除尽,方法是 。
(3)写出操作③有关的化学反应方程式 。操作④的名称是 。
(4)此设计方案是否严密,说明理由  。
。
(5)原固体样品中含NaCl m1 g ,最后得到的NaCl固体m2 g ,则m1 m2(填“﹥”、“﹤”或“﹦”)