题目内容
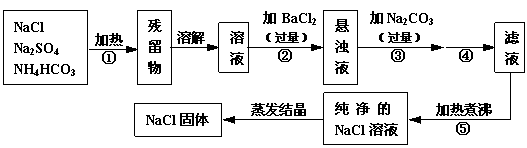
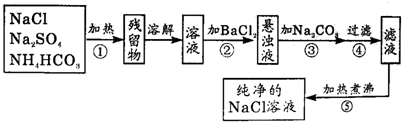
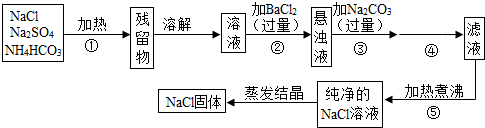
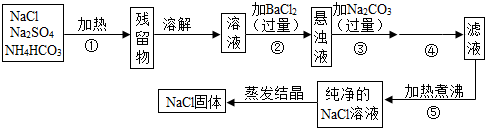
为了将混有硫酸钠、碳酸氢铵(不稳定,受热易分解生成氨气、二氧化碳和水)的氯化钠提纯,某同学设计的实验流程如下:
 |
试回答下列问题:
(1)操作①的目的是 。操作②能否用硝酸钡溶液? (填“能”或“否”)。
(2)进行操作②后,如何判断SO 已除尽,方法是 。
已除尽,方法是 。
(3)写出操作③有关的化学反应方程式 。操作④的名称是 。
(4)此设计方案是否严密,说明理由  。
。
(5)原固体样品中含NaCl m1 g ,最后得到的NaCl固体m2 g ,则m1 m2(填“﹥”、“﹤”或“﹦”)
(1)除去碳酸氢铵(1分);否(1分);
(2)静置,往上层澄清液中滴加BaCl2溶液,如果没有白色沉淀产生,则SO 已除尽(1分);
已除尽(1分);
(3) BaCl2 +Na2CO3==BaCO3↓+ 2NaCl(2分) ;过滤(1分);
(4)不严密,操作③引入的过量Na2CO3没有除去(1分);(5)﹤(1分)。

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
 :
: :
: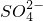 已除尽,方法是______.
已除尽,方法是______.