题目内容
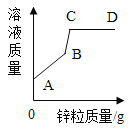
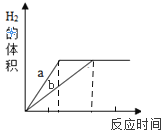
【题目】质量相等的镁和铝分别和等浓度、等质量的稀盐酸反应,反应情况如图所示。则下列叙述中正确的是
A.金属均反应完,盐酸一定有剩余
B.反应结束后,参加反应的镁和铝的质量比为4:3
C.盐酸均反应完,镁一定有剩余
D.图中a、b分别表示铝镁的反应情况
【答案】B
【解析】
设镁和铝质量为m。
A、 x1=
x1=![]() ;
;  x2=
x2= ![]()
可知:等质量的不同金属完全反应生成氢气不会一样多,
![]()
![]() 可知:酸和氢气的质量比都是73:2,等质量的酸生成氢气一样多,图像中氢气一样多,说明是由酸的量决定氢气的质量,即盐酸一定完全反应,选项错误;
可知:酸和氢气的质量比都是73:2,等质量的酸生成氢气一样多,图像中氢气一样多,说明是由酸的量决定氢气的质量,即盐酸一定完全反应,选项错误;
B、由方程式可知,镁和氢气的质量比为24:2=12:1,铝和氢气的质量比为27:6=9:1,反应结束后,参加反应的镁和铝的质量比为12:9=4:3,选项正确;
C. 盐酸均反应完,生成1g的氢气时,消耗镁12g,消耗铝9g,消耗的镁比铝多,铝一定有剩余,选项错误;
D. 镁的活动性比铝的强,图中a、b分别表示镁、铝的反应情况,选项错误。
故选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】甲和乙的溶解度如下表,20 °C时,将甲、乙两种固体各18g,分别加人盛有50g水的烧杯中,充分溶解后,可观察到如图所示的现象,请回答下列问题:
温度/°C | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | 甲 | 35.7 | 36.0 | 36.5 | 37.3 | 38.4 |
乙 | 13.3 | 31.6 | 63.9 | 85.5 | 110 | |
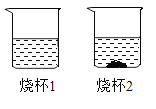
(1)40°C时甲物质的溶解度是_____g。
(2)烧杯1中溶液是_____(填“饱和”或“不饱和”)溶液。
(3)乙物质中含有少量的甲物质,通过_____方法可以提纯乙物质。
(4)将温度升高到80°C,两烧杯内溶液中溶质质量_____(填“相等”、“不相等’或“无法判断”)(不考虑水分蒸发)。