题目内容
某样品为Cu和CuO的混合物,为测定样品中CuO的含量,甲、乙、丙三位学生用同一种样品分别进行实验,测得的数据如表,分析数据,回答问题:
(1)求混合物中氧化铜的质量分数;
(2)求硫酸溶液中溶质的质量分数.
 | 学生甲 | 学生乙 | 学生丙 |
| 所取固体样品的质量/g | 25 | 20 | 20 |
| 加入硫酸溶液的质量/g | 100 | 100 | 120 |
| 反应后剩余固体的质量/g | 12 | 12 | 12 |
(2)求硫酸溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:本题是数据分析题,由乙和丙的数据得出,在此反应中,混合物中的CuO已完全跟酸反应,最后剩余的固体全部为Cu,所以就很容易求出氧化铜的质量分数;根据铜的质量求出氧化铜的质量,然后根据方程式即可求出硫酸溶液的浓度.
解答:解:(1)由乙和丙的数据得出,混合物中的CuO已完全跟酸反应,最后剩余的固体全部为Cu,所以混合物中氧化铜的质量分数为:
×100%=40%
(2)设硫酸溶液的质量分数为x
CuO+H2SO4═CuSO4+H2O
80 98
8g 100x
=
,
解得:x=9.8%
答:硫酸溶液的质量分数为9.8%.
故答案为:(1)40%;
(2)9.8%.
| 20g-12g |
| 20g |
(2)设硫酸溶液的质量分数为x
CuO+H2SO4═CuSO4+H2O
80 98
8g 100x
| 80 |
| 8g |
| 98 |
| 100x |
解得:x=9.8%
答:硫酸溶液的质量分数为9.8%.
故答案为:(1)40%;
(2)9.8%.
点评:本题贵在数据分析,找出已知量,然后利用化学方程式计算,注意解题步骤.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
下列有关催化剂的说法正确的是( )
| A、催化剂只能改变反应速率 |
| B、催化剂在反应前后质量和性质不变 |
| C、催化剂只能加快反应速率 |
| D、催化剂是化学反应的必要条件 |
下列现象或事实,用 分子的相关知识加以解释,其中正确的是( )
| A、热胀冷缩,说明分子大小随温度改变而改变 |
| B、水银温度计放在热水中温度上升,说明汞分子之间有间隔,温度越高,间隔越大 |
| C、水通电后生成氢气和氧气,说明在化学变化中分子可以再分 |
| D、氢气在氯气中燃烧,种类发生了改变的粒子是氢原子和氯原子 |
下列变化中属于物理变化的是( )
| A、电解水 | B、白炽灯发光 |
| C、木材燃烧 | D、食物腐败 |
下列变化中,属于化学变化的是( )
| A、氧气液化 | B、镁带燃烧 |
| C、酒精挥发 | D、水结冰 |
下列变化属于化学变化的是( )
| A、铁钉生锈 | B、香水挥发 |
| C、瓷碗破碎 | D、灯泡发光 |
下列变化中,属于化学变化的是( )
| A、人工降雨 | B、食物中毒 |
| C、酒精挥发 | D、活性炭吸附 |
按如图提供的信息,以下判断正确的是( )
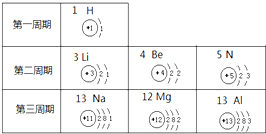

| A、第三周期元素的原子核外电子层数从左到右依次增多 |
| B、第二周期的Li、Be和B均为金属元素 |
| C、Na+和Al3+ 的核外电子数相同 |
| D、Mg2+、H+最外层电子数分别为2和0 |
 在一只盛有稀硫酸的烧杯中漂浮着一块木块,向烧杯中加入适量的某种物质后,木块有所下沉,则加入的固体物质可能是下列物质中的( )
在一只盛有稀硫酸的烧杯中漂浮着一块木块,向烧杯中加入适量的某种物质后,木块有所下沉,则加入的固体物质可能是下列物质中的( )| A、Zn |
| B、Cu |
| C、Ba(OH)2 |
| D、BaCO3 |